ヒントとコツ | siRNAトランスフェクションの最適化
siRNAトランスフェクションは、遺伝子制御や分子経路のメカニズムを解明するために使用されるパワフルなツールです。
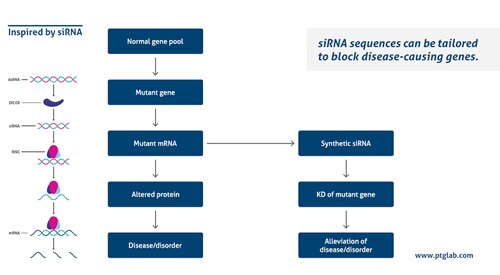
どのように機能するのでしょうか?
悪影響を与えないようにsiRNAを高効率にトランスフェクションする場合、いくつかの異なる要素の検討が必要です。siRNAトランスフェクション(遺伝子導入)を最適化する、以下の10のヒントをご活用ください。
1. プロトコールの最適化
以下の要素は、siRNAトランスフェクションに影響を与えるため、新規に実験を行う際はその都度条件を最適化する必要があります。
- 細胞の種類
- 細胞の増殖速度
- 細胞の密度
- 細胞の生存能力
- トランスフェクション方法
- siRNAの品質/導入量
- トランスフェクション時間
2. RNaseフリーの環境
実験を開始する前に、RNase除去溶液で作業スペースを清掃します。siRNAを扱う時は、常に実験用手袋を着用し、実験台や機器等の表面を触ってしまった場合は実験用手袋を交換します。RNaseフリーのチップを装填したピペットを使用し、これらのピペットは他の実験に使用しないようにします。
3. siRNAの設計
- 約21~23 nt(ヌクレオチド)の長さに設定する
- G/C含量が30~50%になるようデザインする
- 塩基ペアのミスマッチがないこと
- siRNAがイントロンに結合しないようデザインする
- 他の配列と相同性を示す配列がないこと
4. 新規のターゲット/siRNA/細胞株で使用する場合
条件を最適化するために、トランスフェクションを複数回試行する準備をします。
5. コントロールの設定
結果を正しく解釈するためには、適切なコントロールの設定が極めて重要です。
- ポジティブコントロール:目的のターゲットを強くノックダウンする既知のsiRNA
- ネガティブコントロール:サイレンシング効果のないsiRNA(遺伝子発現の非特異的変化を判断する指標となります)
- 同一のターゲットに対する別のsiRNA:同一ターゲットの別のmRNA領域に対する第2のsiRNAによってサイレンシング効果の特異性を確認します。
- 未処理サンプル:トランスフェクションを行わないコントロール実験により、正常な遺伝子の発現レベルを判定します。
- トランスフェクション効率確認用のコントロールsiRNA:蛍光標識したsiRNAを使用すると、使用するsiRNAの導入効率が容易に判明します。
- Mockトランスフェクションコントロール:siRNAを使用せずトランスフェクション試薬で処理した細胞。
6. siRNAデータの検証
- siRNAの用量設定:異なる濃度のsiRNAでトランスフェクションを行います。濃度は製造会社のマニュアルを参考にしますが、通常は5~100nMの範囲で使用します。ノックダウンできる下限値の濃度で実施します。
- RNA発現量、タンパク質発現量のモニタリング監視:mRNAがサイレンシングされていてもそれに付随してタンパク質発現量の低下が認められない場合、タンパク質の代謝回転(ターンオーバー)が遅いことが示唆されます。
7. 細胞培養
トランスフェクション時、細胞は最適な生理条件下にある必要があります。細胞は頻繁に継代培養する必要がありますが、トランスフェクションは常に同一の培養条件下で実施します。通常、トランスフェクション時に約70%コンフルエント程度の高い密度になっている必要があります。しかし、これは細胞の種類によって異なり、実験ごとに判断します。
8. 血清培地と血清フリー培地のどちらを使うか?
ほとんどのトランスフェクション試薬は、siRNA等の希釈に血清フリー培地を使用するステップがあります。トランスフェクションを実施する際、培地に血清が添加されている場合、血清の品質やロット等も実験に影響を及ぼすおそれがあります。
9. 抗生物質添加培地と抗生物質フリー培地のどちらを使うか?
使用する細胞の種類とトランスフェクション試薬の組み合わせによっては、トランスフェクション中は細胞透過性が亢進し、抗生物質に対する感受性が増大します。したがって、抗生物質を添加していると、細胞死の原因となる可能性があります。
10. siRNAサイレンシングの持続期間
一般的に、サイレンシング効果が観察できるのは、早くとも24時間以降です。細胞の種類によっては、4~7日間効果が持続します。
参考文献
K. Huppi et al., Defining and assaying RNAi in mammalian cells. Molcel. 17(1), 1-10 (2005)
Whither RNAi? Nat. Cell. Biol. 5(6), 489-90 (2003)
