ゲスト寄稿 | SARS-CoV-2診断はVHH抗体(Nanobody®)の利用によって進歩する可能性はあるか
Ulrich Rothbauer教授とTeresa Wagner博士課程研究員が新型コロナウイルス(SARS-CoV-2)を認識する「VHH抗体(別名:Nanobody®)」の開発の経緯と、SARS-CoV-2研究におけるその汎用性の高さ、従来型抗体の代替となり得る理由について解説します。
Teresa Wagner、Ulrich Rothbauer著
プロテインテックとクロモテック(2020年よりプロテインテックの一部)は、SARS-CoV-2ウイルスに対するVHH抗体(別名:Nanobody®)の販売を開始しました。製品化された抗SARS-CoV-2 VHH抗体(Nanobody®)は、Ulrich Rothbauer教授(NMI自然医学研究所、ドイツ、ロイトリンゲン)の研究グループによって取得されたクローンに由来する組換え抗体です。本稿では、Teresa Wagner博士課程研究員とUlrich Rothbauer教授がVHH抗体(Nanobody®)の開発の経緯と、SARS-CoV-2研究においてVHH抗体(Nanobody®)が従来型抗体よりも汎用性が高く、代替品となり得る理由を解説します。
従来型抗体の代替品として、汎用性の高いVHH抗体(Nanobody®)
新型コロナウイルス感染症(COVID-19:Coronavirus disease 2019)のパンデミック(世界的大流行)は、前例のない苦難をもたらし、容易に終息には至りませんでした。SARS-CoV-2と命名された新型コロナウイルスに対する初のワクチン開発を目指す世界規模の取り組みの中、パンデミックを克服するための挑戦の一環として基礎研究が注目を集めています。本稿で述べるVHH抗体は、「ナノボディ(Nanobody®)」という名称でもよく知られる単一ドメイン抗体であり、その汎用性が明らかになってきました。
2020年3月、研究グループは個々の免疫応答の血清学的検査のために用いるウイルス特異的抗原の作製を目指し、SARS-CoV-2のスパイク(S)タンパク質の断片を哺乳類宿主で発現させる研究を開始しました。その他方で、基礎研究で使用するための高い親和性を示すSARS-CoV-2の捕捉ツールの確保も急務とされており、COVID-19の治療に向けた中和抗体も必要とされていました。そこで、免疫用の抗原としてSARS-CoV-2のスパイク(S)タンパク質内の受容体結合ドメイン(RBD:Receptor-binding domain)を使用し、SARS-CoV-2特異的なアルパカ由来VHH抗体を産生する研究に取り組むことにしました。受容体結合ドメイン(RBD)は免疫原性が高いことが示されています。免疫原性の高いタンパク質を使用することによって、様々なアルパカ由来VHH抗体の候補を特定することができ、その中には10-9M(nM、ナノモーラー)レベルの高い親和性を有する抗体も含まれていました。
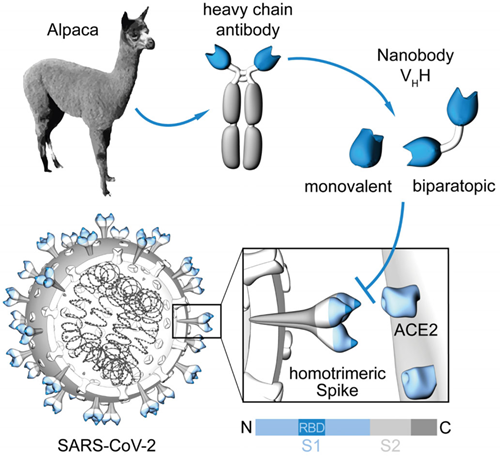
SARS-CoV-2 RBD‐ACE2結合を阻害するアルパカ由来VHH抗体の作製(T Wagner et al. EMBO Rep. 2021より引用)
アルパカ由来VHH中和抗体の単離
宿主細胞(ヒト)のSARS-CoV-2受容体であることが分かっているACE2(angiotensin-converting enzyme 2、アンジオテンシン変換酵素2)とウイルスの相互作用を阻害するアルパカ由来VHH中和抗体を探索するために、VHH抗体が結合する複合体の詳細な特性解析を開始しました。SARS-CoV-2の従来株(オリジナル株)を使用したin vitroのACE2競合アッセイ、ウイルス中和試験(VNT:virus neutralization test)を実施後、HDX-MS(水素‐重水素交換質量分析)によってRBDのエピトープを認識する中和活性の高いアルパカ由来VHH抗体を5種類選抜しました。それらの抗体の中には、ACE2の相互作用部位と直接結合する抗体や、その他の部位をエピトープとして認識する抗体が含まれていました。
さらに選抜した2種類の抗体クローンである「NM1230」と「NM1226」について、アルパカ由来VHH抗体‐RBD複合体の結晶構造解析を実施したところ、エピトープとの結合様式や重要なアミノ酸残基等に関する新たな情報が明らかになりました。「NM1230」は、アルファ(α)株、ベータ(β)株、デルタ(δ)株のような懸念される変異株(VOC:Variants of concern)に認められるK417、L452、E484等の免疫回避に働く変異部位にあたるRBDのアミノ酸残基と直接的に相互作用することが明らかになりました。一方、「NM1226」は、変異株間で共通する進化的に保存されたエピトープと結合します。
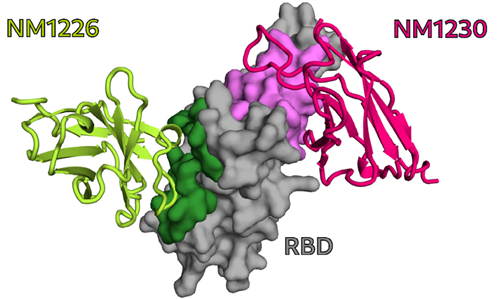
RBDのエピトープと結合するNM1226、NM1230(T Wagner, et al. EMBO Rep. 2021より引用)
バイパラトピックVHH抗体の作製
研究で示された結果から、両方のVHH抗体を1つの分子として融合し、2種類の異なるエピトープに対する結合特性を有する「バイパラトピックVHH抗体(bipNb:biparatopic nanobody)」の作製を考案しました。「NM1267」と命名されたbipNbは、ウイルス中和アッセイでKD=480pMおよびIC50=890pMを示す、著しい親和性の増加を示しました。驚くべきことに、NM1267は現在報告されている変異株(VOC)すべての各RBDに対して、それぞれに同程度の効率で結合しました。
「NeutrobodyPlex」による中和抗体の検出
バイパラトピックVHH抗体(bipNb)を血清学的競合リガンド結合アッセイに組み込んだ「NeutrobodyPlex」による評価を実施しました。中和抗体とスパイクタンパク質間の相互作用に対して、bipNb添加による置換を検出することで、COVID-19感染者やワクチン接種者の血清サンプル中の中和抗体量をハイスループットに測定することができました。NeutrobodyPlexは、感染患者が再感染を防ぐための中和抗体を産生しているのか否か、あるいはワクチン接種者が免疫を獲得しているか否かを評価する等の用途に用いることができます。特筆すべきは、この間接的な抗体量測定法は、様々な濃度のサンプルで迅速に結果を得ることが可能で、ラボがウイルス中和試験(VNT)を実施するにあたって従来の事例で求められていたBSL3レベルの安全性の要件を満たしていなくても実施が可能という点です。
まとめ
本研究は、SARS-CoV-2特異的なアルパカ由来VHH抗体の作製方法と、中和免疫応答の診断検査への応用可能性を示しました。従来型抗体と比較して、アルパカ由来VHH抗体は、認識エピトープに関する正確な知見、マルチパラトピックなVHH抗体を作製できる柔軟性、産生の容易さといった、数々の利点があります。アルパカ由来VHH抗体は、一般的に高温耐性があり、長期にわたり安定性を示すという特徴を有しており、アルパカ由来抗SARS-CoV-2 VHH抗体は、サロゲート物質、捕捉試薬、検出試薬として最適な診断用ツールに応用できる可能性があります。この成果を発表後、研究グループはbipNbを用いた治療の可能性を明らかにするための研究を開始しました。これまでの結果は、これから投与容易な予防薬やSARS-CoV-2感染者の治療薬としてさらにbipNbを開発していくことに大きな自信をもたらすものとなっています。
補足:VHH抗体(Nanobody®)について
従来型抗体(IgG、免疫グロブリンG)は、2本の長鎖タンパク質(重鎖)と2本の短鎖タンパク質(軽鎖)で構成され、これら4本のタンパク質鎖で特徴的なY字型構造を形成します。重鎖と軽鎖の末端に存在する抗体の可変領域は、ほぼ全てのターゲット物質に対して各抗体独自の結合特性を付与します。抗体は進化的に高度に保存されたアミノ酸配列を有しています。例外的に、ラクダ、アルパカ、ラマ等のラクダ科動物は「愛らしくふわふわしている」だけでなく、通常の免疫グロブリンとは異なる形状の「重鎖抗体(HCAb:heavy chain only antibody)」と呼ばれる免疫グロブリンを有していることをブリュッセル自由大学の研究者らが1993年に見出しています。この発見は、世界に大きな驚きと関心をもたらしました。注目すべきことに、重鎖抗体は、単一の可変領域からなるにもかかわらず、ターゲットとの結合部位は完全な機能性を有していました。重鎖抗体は非常に小型(直径2.5nm、全長4nm)であることから、2001年にAblynx社(現Sanofi社傘下)はこの単一ドメイン抗体フラグメントを「ナノボディ(Nanobody®)」と命名・商標登録し、以後この名称が一般的な名称としても浸透しています。VHH抗体(Nanobody®)は高い溶解性、熱安定性、化学的安定性、良好な組織浸透性、低い免疫原性等の特性を有します。さらに、VHH抗体(Nanobody®)は容易に遺伝子改変を行うことができ、高いアビディティ(Avidity:2つ以上または複数の抗原結合部位が標的抗原エピトープと同時に相互作用することによって生じる累積結合強度または機能的親和性)を示す、あるいは任意のマルチ特異性を示す、変異体/マルチパラトピック抗体を作製することができます。VHH抗体(Nanobody®)は、大腸菌等の発現宿主に組換え発現ベクターを導入する産生手法を採用しているためコスト効率に優れ、生物医学研究、診断用アプリケーション、治療用アプリケーション等における従来型抗体の魅力的な代替分子であるといえます。
著者情報
Teresa Wagner博士課程研究員、Ulrich Rothbauer教授
Tübingen大学NMI自然医学研究所(ドイツ、ロイトリンゲン)
参考文献
関連情報
Scientists unravel why Omicron spreads faster
Neuropilin-1 joins ACE2 as SARS-CoV-2 gateway
Neutralizing antibodies and their role in COVID-19 research
How fluorescent proteins can be applied in SARS-CoV-2 research
Serious about Serology: Understanding COVID19 Antibody Tests
Characterization of COVID-19 antibodies by Bio-Layer Interferometry using Nano-CaptureLigands



