免疫蛍光染色とパッチクランプ法による皮質細胞の種類の同定
Airi Watanabe著(McGill大学、Ph.D. Candidate)
|
目次 |
大脳皮質
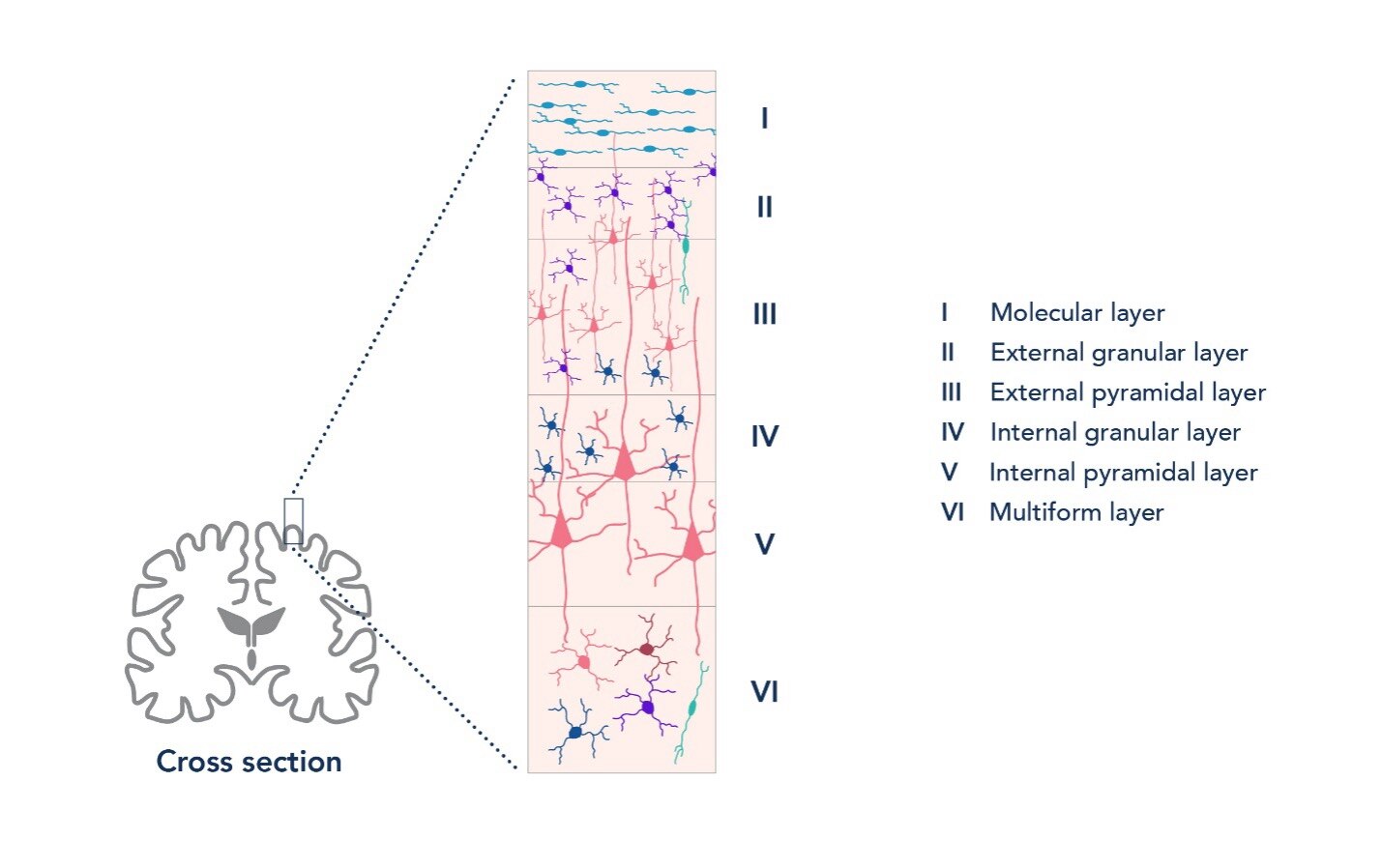
大脳皮質とは脳の最外層領域を指し、神経細胞とグリア細胞が混在しています。大脳皮質は認知機能を司り、記憶・注意力・意識等に関与します。また、視覚を司る視覚野や感覚を司る体性感覚野のように、皮質領域ごとに様々な特定の機能を担っています。大脳皮質の約90%を占める大脳新皮質は、下図のように6つの水平な層で構成されており、ニューロンは大脳皮質の機能的柱状構造内に放射状に配列しています。
|
図1. 新皮質は6つの皮質層からなり、層ごとに神経細胞の種類と構成が異なります。 |
特定の機能を発揮するために、皮質には特殊な機能を担う様々な細胞を含む回路が形成されています。皮質ニューロンには投射ニューロンと介在ニューロンという主要な2種類のニューロンが存在します。皮質内の投射ニューロンの大部分は興奮性錐体細胞で、皮質ニューロン全体の約80%を占めています。介在ニューロンは主に抑制性機能を有する様々な細胞群を指し、バスケット細胞やマルティノッティ細胞等が含まれます。
異なる種類の神経細胞が協調することで皮質回路は適切に機能します。皮質に存在する興奮性細胞と抑制性細胞による興奮性/抑制性活動の均衡の破綻はてんかん等の神経病態の大きな特徴で、統合失調症等でもその関連が認められています。多種に及ぶニューロンの存在を鑑みると、細胞特有の機能を解明できれば、神経疾患を精密に治療可能な医薬品等の開発を促すと考えられます。したがって、生理的・病理的条件下における皮質の接続性や機能を研究するにあたっては、神経細胞を具体的に同定する必要があります。
パッチクランプ法入門
神経科学の分野では、生理機能を維持した状態のニューロンの電気的活動を計測するために電気生理学(略:Ephys)の手法を利用します。パッチクランプ(Patch-clamp)法は、Bert SakmannとErwin Neherによって考案・確立された電気生理学の代表的手法で、個々の細胞の膜電位の精密な変化を研究するために広く用いられています。
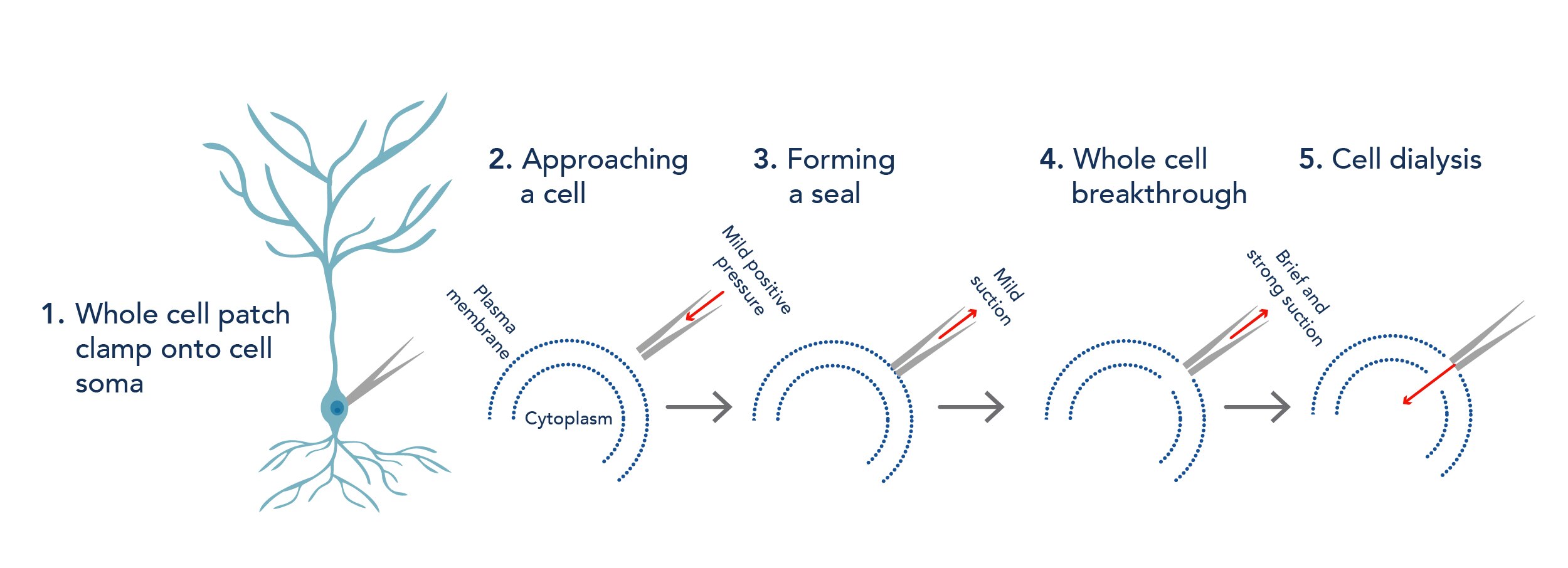
本稿では、パッチクランプ法の中でも、急性脳スライス標本(Acute brain slice)のWhole-cellパッチクランプ法について解説します。この手法では、(1)細胞内液の組成を模倣した溶液を充填したガラスピペットを使用して細胞内にアクセスし、(2)ピペットを細胞に近づけ、(3)ピペット内に軽い陰圧をかけて細胞膜に「シール」を形成します。(4)シールが形成されたら、さらに陰圧をかけパッチ膜を破って細胞質にアクセスします。その後、(5)ピペット内の溶液を細胞に拡散・置換し、膜電位の変化の計測や膜電位の実験的制御を行います。Whole-cell法以外にも、パッチクランプ法にはCell-attached法やPerforated-patch法といった多様な手法が存在します。細胞の電気的変化を計測することで、例えば、細胞の学習に関わる可塑性の機構、神経疾患によって脳細胞の接続性が変化する機構、脳細胞に対する薬剤の作用等を調べることができます。
|
図2. Whole-cellパッチクランプ法の主要なステップ |
皮質細胞の電気的活動を記録する際のポイント
-
記録用の脳スライス標本を適切に作製するよう留意します。実験日ごとに新たにスライス溶液を作製する、細胞の形態を維持したスライスになるように薄切時の厚さや角度を検討するといった点に留意しましょう(例:錐体細胞の尖端樹状突起)。
-
適切な深さに存在する細胞を選んでパッチを行い、スライス標本作製時に生じる表面壊死層の変性細胞や、切片の深部に存在し観察が困難な細胞を測定しないようにします。
-
ガラスピペットは記録を行う当日に作製してください。ガラスピペットでパッチする際に、ほこりやガラスの破片等の異物がピペットの先端に目詰まりするのを防ぐことができます。
-
パッチクランプ法に使用する実験装置は適切に維持管理しましょう。留意事項としては、バスチャンバー周辺に飛び散った液体は掃除すること、ケーブルを適切に管理すること、電極(銀線)の塩化銀コーティングを定期的に行うこと等が挙げられます。
-
場合によっては、何度もパッチを試みる必要があります。パッチクランプを実施しようとした細胞が変性細胞のようであれば(例:シールを形成できない、静止膜電位が非常に脱分極した状態にある)、別の細胞に対してパッチクランプを実施するか、別のスライス標本を使用しましょう。
大脳皮質の細胞を判別する方法
電気生理学的特性
細胞の種類を同定する方法の1つは、パッチクランプ法で持続的に電流を注入(~500 ms)した際の電気生理学的特性を確認するという方法です。グリア細胞の多くは受動的な膜特性を有し、脱分極性の正電流を注入しても活動電位が発生しないため、容易に神経細胞と区別できます。また、神経細胞はそれぞれの細胞の活動電位の発火パターン(スパイク)に基づいて同定できます。
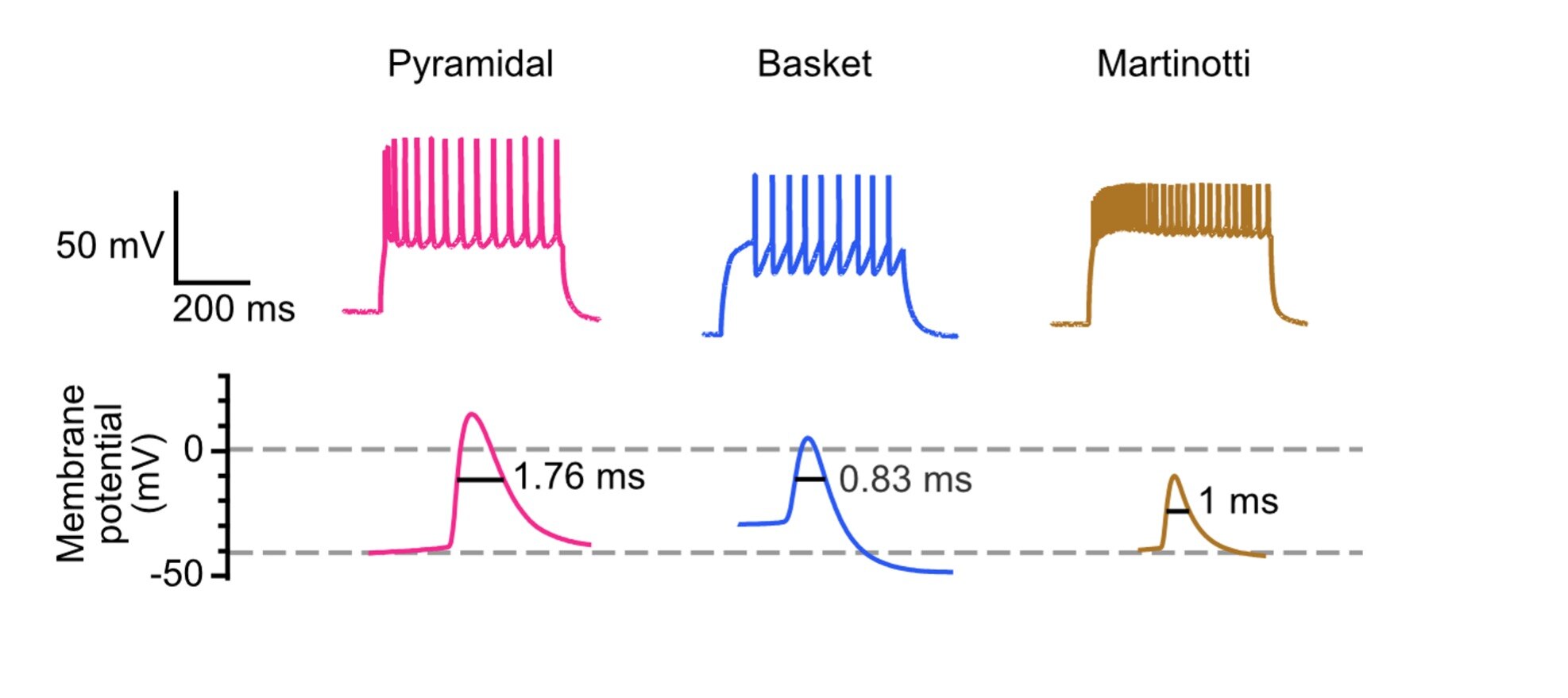
錐体細胞は順応性のスパイクパターンを示すことが知られています。つまり、持続的に電流注入し活動電位の連続発火が誘発されると、錐体細胞は後続の活動電位が発生する(発火する)までの間隔が長くなります。バスケット細胞等の一部の細胞は非順応性のパターンで、高頻度の活動電位を示します(例:Fast-spiking)。ただし、このような細胞を同定する目安になる情報は存在するものの、異なる種類の細胞が同じようなスパイクプロファイルを示す場合があるため、パッチクランプ法による解析だけでは細胞の種類を確実に判定できません。例えば、錐体細胞とマルティノッティ細胞は両者とも順応性のスパイクパターンを示します。したがって、パッチクランプ法と併用して、細胞の種類を詳細に解析できる他のアッセイを実施することが推奨されます。
|
図3. スパイクパターンやスパイク半値幅等の電気生理学的特性は、皮質細胞の種類を同定するための参考情報として用いられます。 |
形態解析
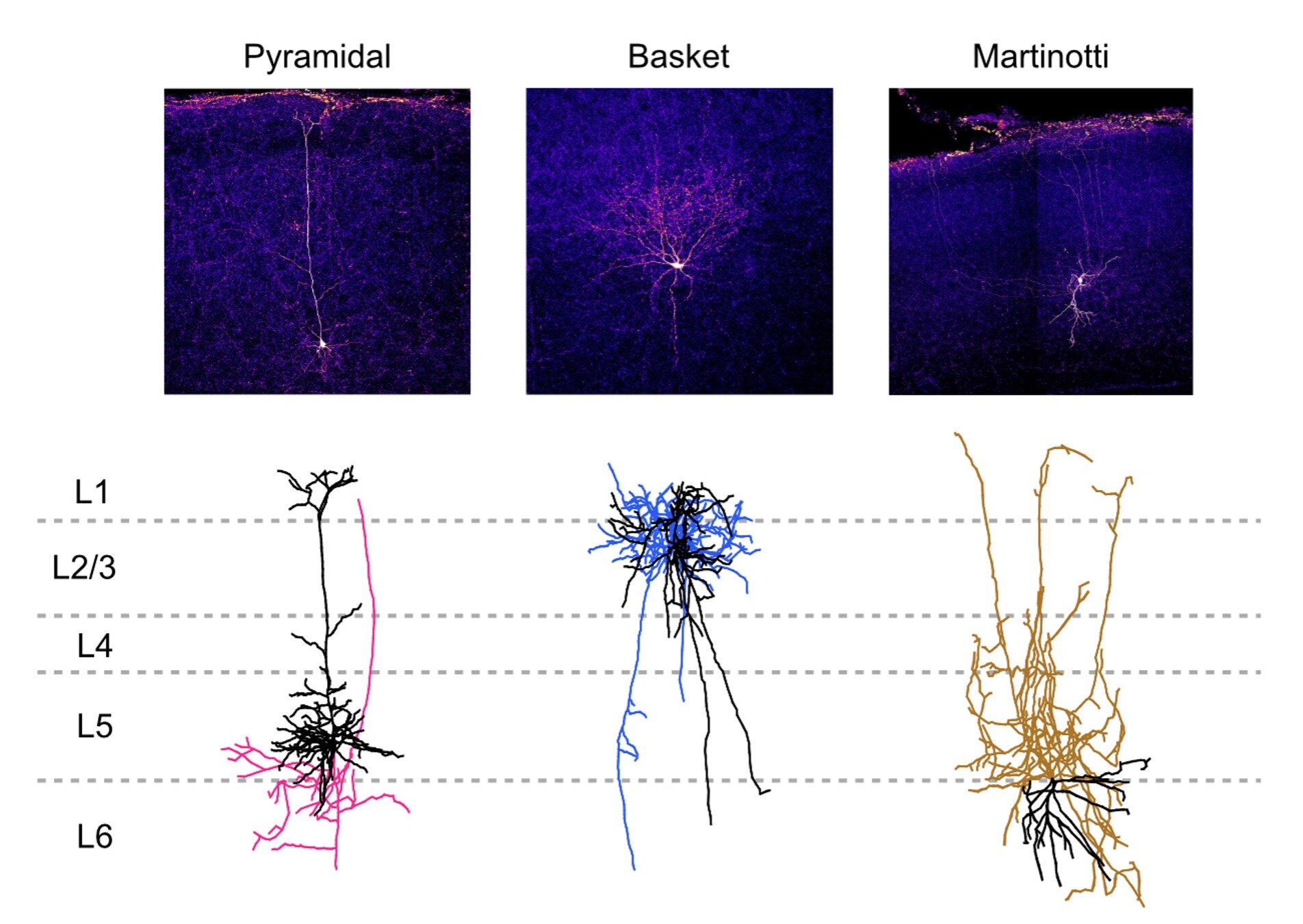
パッチクランプ法による測定と形態解析を併せて行うと、細胞の機能と構造を関連づけて調べることができます。形態解析を実施する場合は、パッチピペットの内液にあらかじめバイオサイチンやビオチンを添加し、パッチした細胞にこれらの分子を拡散させます。そして、蛍光物質を標識したストレプトアビジンやアビジンを使用して、細胞内のバイオサイチン・ビオチンを検出します。この手順で、例えば共焦点顕微鏡のような顕微鏡下で細胞形態を可視化することが可能になります。一般的に、共焦点顕微鏡観察では電気生理学的実験に用いる顕微鏡よりも解像度の高い情報が得られます。また、トレースソフトウェアを使用すると、取得した画像スタックから細胞形態を3D画像に再構成できます。このような構造解析用ツールを利用すると、再構成された3D情報から細胞の種類を同定できます。
|
図4. 様々な神経細胞のバイオサイチン染色画像(上図)と形態学的再構築像(下図、黒線:樹状突起、色つき線:軸索)。この実験では、再構築像を皮質細胞の種類を特定するための参考情報として利用しています。画像提供:Christina Chou博士、Cleo Huang、Tal Klimenko、Vivian Wu(McGill大学)。 |
免疫蛍光染色
いくつかの細胞特異的なマーカーを組み合わせて免疫蛍光染色を行うと、細胞の種類を詳細に同定できます。パッチクランプで記録した細胞の種類を確認するために、免疫蛍光染色を単独で実施するか、バイオサイチン染色を併せて実施します。
神経細胞はその種類に応じて特定の異なるマーカーを発現しているため、各細胞の特徴的なマーカーを抗体で検出します。例えば、皮質錐体細胞はCaMKIIで同定します。バスケット細胞はパルブアルブミン陽性細胞であるため、この種類の細胞は抗パルブアルブミン抗体を使用して確認します。グリア細胞も皮質を構成する細胞です。抗体を使用すると、グリア細胞の種類をさらに詳細に同定できます。以下の一覧表には、一般的な皮質細胞とよく利用されるマーカーをまとめました。
|
種類 |
代表的なマーカー |
|
錐体細胞(Pyramidal cell) |
|
|
バスケット細胞(Basket cell) |
|
|
マルティノッティ細胞(Martinotti cell) |
|
|
VIP陽性細胞(VIP interneuron) |
|
|
アストロサイト(Astrocyte) |
|
|
ミクログリア(Microglia) |
|
|
オリゴデンドロサイト(Oligodendrocyte) |
CNPase、PLP1 |
|
オリゴデンドロサイト前駆細胞(Oligodendrocyte precursor cell) |
表1. 主要な皮質細胞の同定に用いられる一般的なマーカー
Whole-cell法で記録した細胞に対して免疫蛍光染色を実施する場合、記録中に特定の細胞質マーカーがピペット側に拡散し、染色シグナルが減弱する場合があるという点に留意します。パッチクランプ法によって長時間の記録を実施した後に免疫染色する際は、この点に特に注意してください。この問題の影響を受けることが多いマーカーとして、パルブアルブミン、カルビンジン、カルレチニン等が挙げられます。
まとめ
大脳皮質に存在する様々な種類の細胞間の相互作用は、皮質回路の適切な機能に寄与しています。本稿で述べた手法を使用すると、細胞の種類を正確に同定し、神経疾患等の病態への理解を深めることができます。Cre-Lox遺伝子組換えシステムや光遺伝子制御技術のような高度な技術と上記のツールを組み合わせると、皮質の接続性や機能の研究も行えるようになり、脳の解明がさらに進むと考えられます。
|
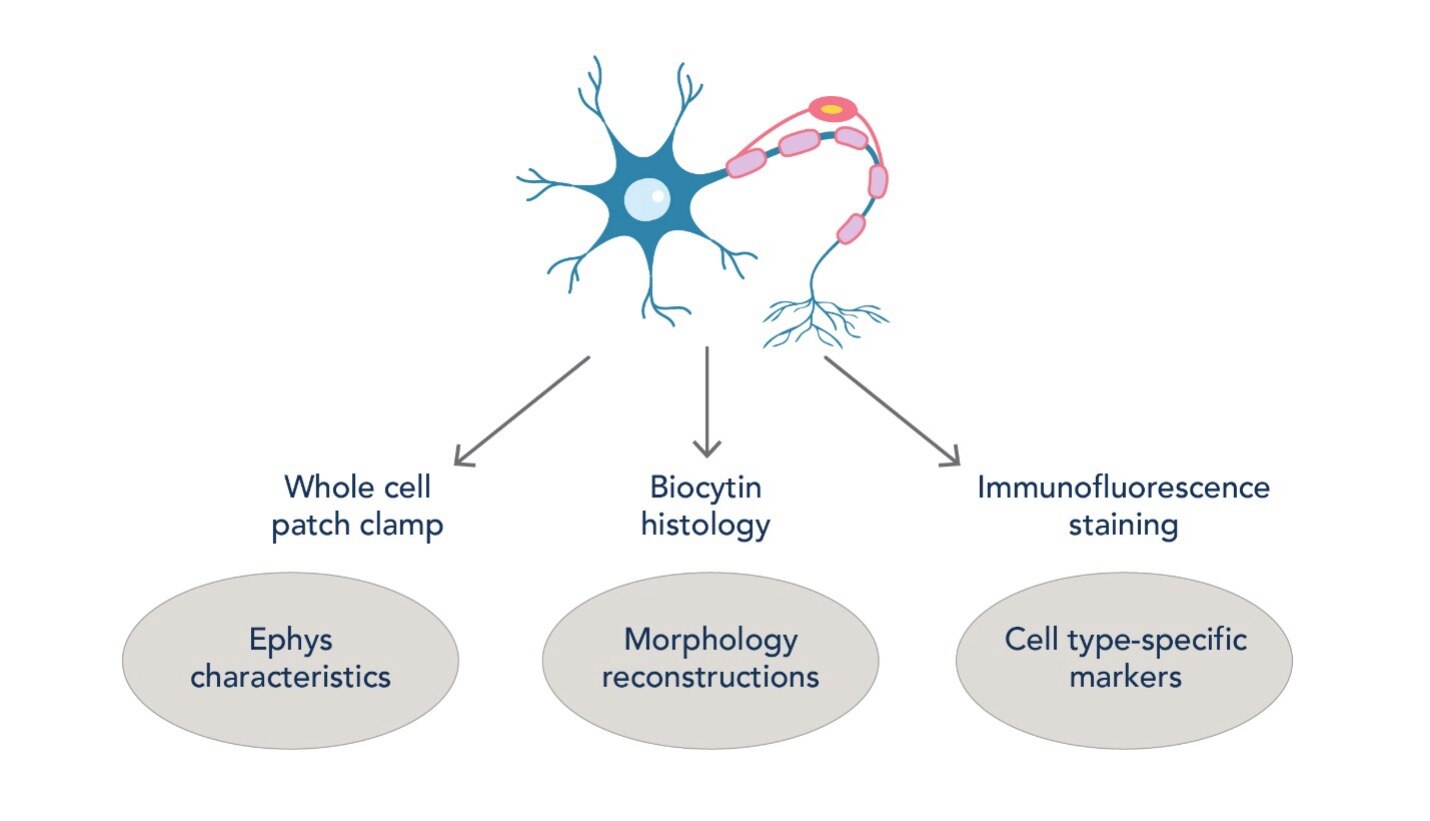
図5. 電気生理学的手法、形態学的手法、免疫染色法を組み合わせて、大脳皮質の細胞の種類を同定するワークフロー。大脳皮質の微小回路を細胞の種類に応じて高い精度で研究するうえで、このような技術が大いに貢献します。 |
参考文献