SARS-COV-2の感染機構としてNEUROPILIN-1がACE2に加わる
プロテインテックとChromoTekの抗体を使用して、Neuropilin-1がSARS-CoV-2の宿主細胞侵入に必要であることを詳述した画期的な論文がScience誌に発表されました。
現在のCOVID-19(コロナウイルス感染症2019)のパンデミックは、SARS-CoV-2(重症急性呼吸器症候群コロナウイルス2)の感染によって引き起こされています。SARS-CoV-2に関する研究は驚くほど膨大にもかかわらず、ウイルスの侵入機構に関する多くの疑問が残されています。現時点では、SARS-CoV-2のS(スパイク)タンパク質が最初に宿主細胞膜上のACE2(アンジオテンシン変換酵素2:Angiotensin-converting enzyme 2)受容体と結合するという共通認識で一致しています。その後、Ⅱ型膜貫通型セリンプロテアーゼであるTMPRSS2とHAT(human airway trypsin-like protease)がSタンパク質を開裂してSタンパク質を活性化すると、ウイルス膜融合が開始し、それに伴いウイルスRNAが宿主細胞へ侵入します。また、プロテアーゼであるフーリン(furin)がSタンパク質をS1サブユニットとS2サブユニットに切断することで感染性を増大させることが示唆されています。Science誌に同時に掲載された画期的なDalyらの論文とCantuti-Castelvetriらの論文では、SARS-CoV-2のウイルス侵入機序における新規メディエーターとして、Neuropilin-1の役割が述べられています(PMID:33082294、33082293)。本論文により、Neuropilin-1は、呼吸器系細胞や嗅覚系細胞に多く発現し、フーリンにより切断され生じるS1中のモチーフと細胞表面で結合して宿主細胞への侵入性を増強させる能力を有することが示唆され、これら臓器系に対するウイルスの親和性に関与する可能性について示されました(図1)。
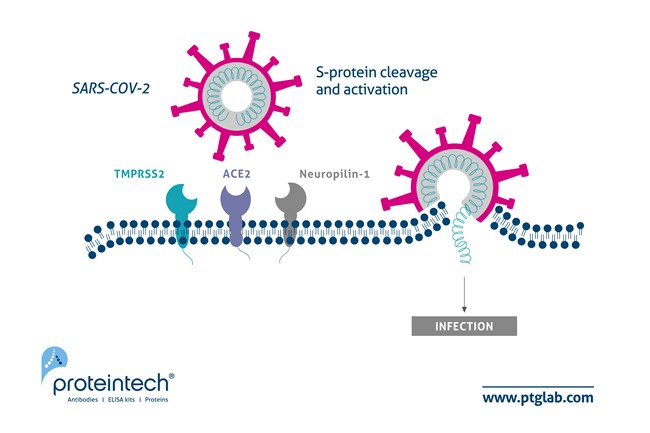 |
| 図1. Neuropilin-1を追加したSARS-CoV-2宿主細胞侵入の最新の概略図。 HeurichらによるJournal of Virologyの論文の図を改変しています(PMID: 24227843)。 |
Neuropilin-1が細胞への侵入に影響を及ぼすかどうかを確認するため、Cantuti-CastelvetriらはACE2、TMPRSS2、Neuropilin-1を別々の組み合わせでトランスフェクションした細胞に対してSARS-CoV-2の感染性を試験しました。Neuropilin-1を単独で発現させると、細胞は感染に至りませんでした。しかし、Neuropilin-1をACE2およびTMPRSS2と共発現させた場合、ACE2およびTMPRSS2のみの組み合わせで共発現させた場合よりも感染性が顕著に増大しました。さらに、これらの細胞をNeuropilin-1の結合部位を機能的に阻害するモノクローナル抗体で処理すると、感染率は有意に低下しました。その際、研究者らはSタンパク質のフーリン結合部位を欠くSARS-CoV-2を作製しました。この変異株は、ウイルス受容体を共発現させた細胞での感染が増大せず、Neuropilin-1がその作用を発揮するにはフーリンによって切断されたSタンパク質との結合が必要であることが確認されました。続いて、フーリンによる切断を受けたSタンパク質のC末端配列からなるペプチドを作製し、マウス嗅上皮へin vivo投与するために銀ナノ粒子(AgNP)と結合させました。投与して6時間後、コントロールペプチドと比較して、AgNP結合Sタンパク質ペプチドの取り込みの有意な増加が認められました。最後に、Cantuti-Castelvetriらは重症のCOVID-19患者から得た気管支上皮細胞のトランスクリプトーム解析を実施しました。これらの患者では、Neuropilin-1、TMPRSS11a、フーリンのRNA発現量は有意に増加していました。興味深いことに、ヒト肺上皮におけるNeuropilin-1の免疫反応性は、ACE2と比較して非常に高く、ACE2はほとんど検出できなかったことから、Neuropilin-1は発症に関して高い役割を担っていることが示唆されました。この研究は、ウイルス-宿主細胞相互作用を円滑化するNeuropilin-1の役割の重要性と、COVID-19の今後の治療における新たなターゲットとしての可能性を示唆しています。
また、同時に掲載されたDalyらの論文では、プロテインテックのACE2モノクローナル抗体(カタログ番号:66699-1-Ig)が使用されています。in vitroでのSARS-CoV-2感染モデルとして使用されたHEK-293細胞におけるACE2の過剰発現を定量するためのウェスタンブロットに使用されました。
ChromoTek(クロモテック:2020年よりプロテインテックの一部)のGFP-Trap®およびRFP-Trap®は、GFPまたはmCherryタグ融合タンパク質、またはSタンパク質発現VSV(水疱性口内炎ウイルス)シュードタイプウイルスのCo-IP(共免疫沈降)に使用され、その後ウェスタンブロットで定量化されました。例えば、mCherry-b1 Neuropilin-1やmCherry-b1 T316R変異体Neuropilin-1をHEK293T細胞で発現させ、RFP-Trap®でプルダウンして回収しました。RFP-Trap®によるmCherry標識タンパク質の濃縮後、Sタンパク質発現VSVシュードタイプウイルスをさらにRFP-Trap®ビーズに添加して、ウイルスのCoIPを実施しました。この手順により、著者らはGFP標識タンパク質やmCherry標識タンパク質の一般的な精製操作をスキップしました。代わりに、細胞ライセートからタンパク質をビーズ上で捕捉し、捕捉したタンパク質を使用してウイルスとの相互作用の解析やタンパク質量の定量を実施しました。
ACE2抗体やNeuropilin-1抗体等のCOVID-19に関連する試薬は、COVID-19の特集ページ(ptglab.co.jp)でご覧いただけます。ChromoTekのVHH(Nanobody®)試薬に関する詳細情報はこちら(Proteintech VHH(Nanobody®)試薬)をご覧ください。
