水晶振動子微小天秤:次世代バイオセンサーとしての可能性
水晶振動子微小天秤(QCM)は次世代バイオセンシングを牽引する可能性のある有望な技術として注目されています。本稿ではバイオマーカー検出を中心に、その基礎となる原理を解説します。
Benjamin Raven著(英国Sheffield大学、生化学専攻、博士課程在籍)
材料科学やナノテクノロジーの分野は、生物学の分野に多大なインパクトを与える可能性があり、ナノスケールレベルの物質制御や事象の解明を介して画期的なイノベーションや科学的発見を後押しできると考えられています。水晶振動子微小天秤(QCM:Quartz Crystal Microbalance、水晶振動子マイクロバランス)は、センサー表面の分子挙動を詳細に追跡できる有力な手段です。QCMは物理学・化学・工学の諸分野を横断する手法であり、分子結合・吸着・薄膜堆積に基づいた独自の解析手段で分子動態を解明します。この手法によってセンサー表面の微細な質量変化の詳細な解析・定量能力は飛躍的に向上し、基礎科学から、バイオセンシング技術・材料コーティング技術等の最先端の応用科学にいたるまで様々な知見をもたらしています。
QCM法概論
QCM法は、センサー表面の質量変化を計測する技術です。QCMは1960年代から膜厚や質量変化を計測するために用いられていましたが、分子生物学の分野で解析に用いられるようになったのは比較的最近です。Stanley Bruckenstein博士・Michael Shay博士による1985年の論文「Experimental aspects of use of the quartz crystal microbalance in solution.[1]」は、QCMを用いた生物試料の計測という新たな可能性を示しました。この時点までQCMは真空下で実施する必要がありましたが、液相中での測定技術が導入され、センサー表面に生物試料を通過させることが可能になり、特定の分子が表面修飾されたセンサーへのバイオアナライトの結合を計測できるようになりました。
|
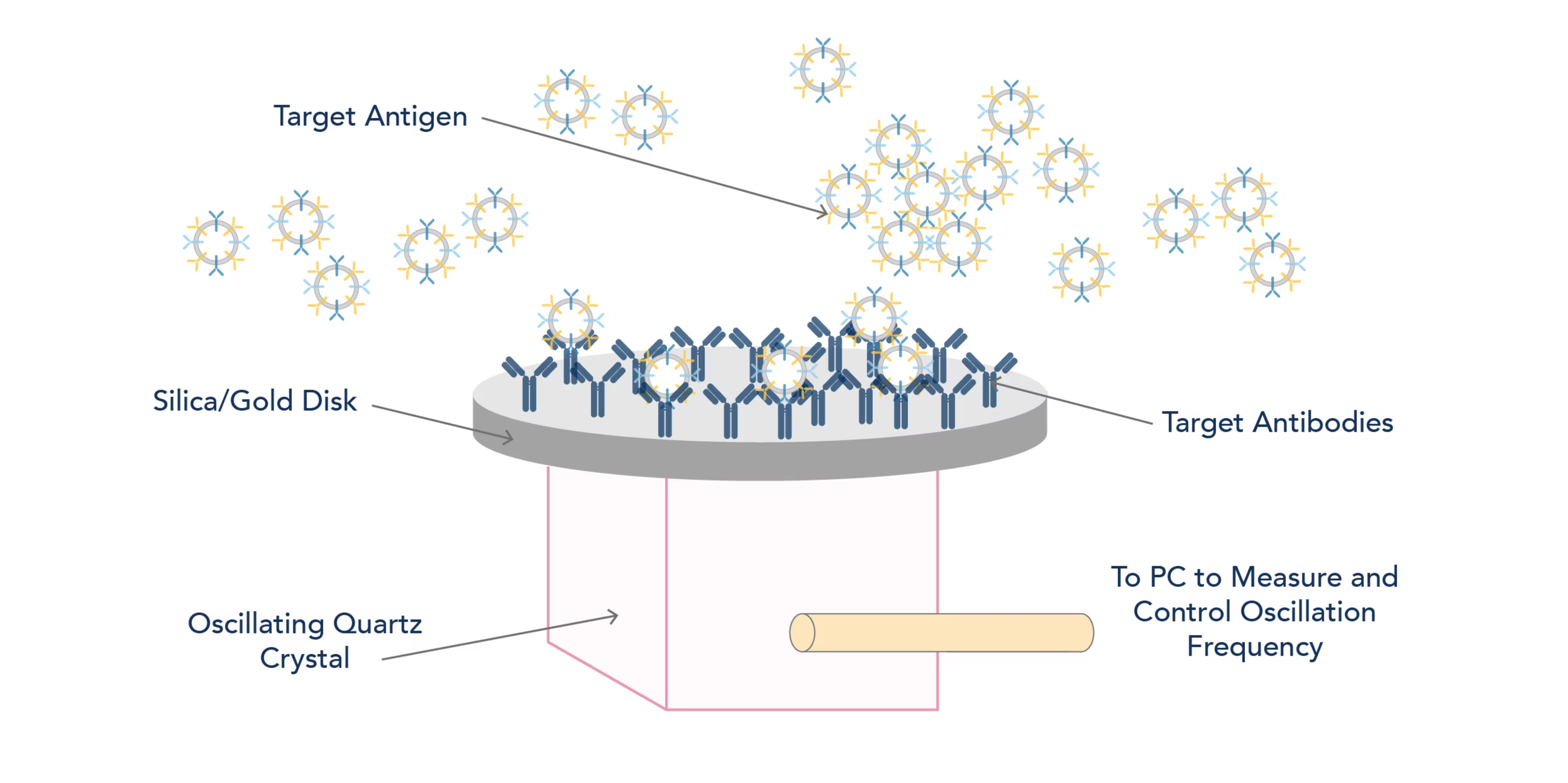
図. QCM図解 |
QCMの動作原理
QCMは、金属薄膜を成膜した板状の水晶の圧電効果を利用する技術です。圧電効果とは特定の素材に機械的応力を加えると電圧(電荷)が発生する現象を指します。物理的な圧力によって電圧が発生する原理は、圧電点火装置(例:BBQライター)や構造物の変形を計測するためのひずみゲージ等に応用されています。圧電効果は可逆的であり、電圧をかけることで圧電素材が振動する逆圧電効果という現象も存在します。逆圧電効果の原理はクオーツ時計やコンピューター等の電子機器の内部時計に応用されています(クオーツ時計は水晶振動子の振動を時間精度の管理に利用します)。AFM(原子間力顕微鏡)プローブやQCMを採用した精密機器は、逆圧電効果によって発生する水晶振動子の極めて正確な振動を利用しており、QCMを用いた検出機器は、表面に分子修飾を施した金属薄膜に交流電圧を印加して水晶振動子を特定の振動数(通例:5 MHz)で発振させ、薄膜上の質量負荷による振動数の減少を計測することで、ナノグラムレベルの質量変化を算出します。
質量センサーとしてのQCM
水晶振動子の振動数変化量は水晶振動子の質量変化量に比例する(Sauerbrey方程式)というのが、QCMの根本的な物理学的原理です。抗原抗体反応等を介して分析対象物質が水晶上の金属薄膜に結合すると水晶センサー表面の質量が変化し、たとえ微細な質量変化であっても検出系が測定可能なレベルの振動数変化が生じます。そこで、試料添加等に伴う振動数の変化を追跡し、液体の粘性負荷を考慮し液相測定用に改変したSauerbrey方程式を用いて質量変化を算出します。Sauerbrey方程式の物理パラメータの多くは一定であるため(例:水晶密度・水晶のせん断弾性率)、この方程式はPython等のプログラミング言語を利用すると瞬時に計算できます。QCM法は質量を直接測定する手法ではありませんが、振動数の変化から水晶振動子表面の質量増減を導き出せるため、質量変化を計測する質量センサーとして応用されています。この質量増減は、素材表面の浸食[2]や薄膜堆積[3]の他、水晶振動子上の薄膜への分析対象物質の結合等の様々な現象により生じます。水晶振動子薄膜にターゲットを捕捉する抗体を修飾すれば、サンプル中の抗原の有無を高感度に検知することが可能になります。
バイオマーカー検出におけるQCMの活用
QCMはバイオマーカーの探索や検証試験に特に有用な技術です。ストレプトアビジンを結合させ機能性を付与した水晶振動子薄膜センサーを用いれば、C末端側またはFc領域を特異的にビオチン化したビオチン標識抗体を抗体のN末端側を溶液に向けた配向で薄膜表面に捕捉することができます。可変領域が存在するN末端が溶液側に面した配向になると、薄膜上を試料が通過する方向に抗原結合部位が露出し、抗原と抗体の結合反応が促進されることで検出感度が向上します。抗体ベースのイムノセンサーを用いる場合、試料には細胞外小胞・微生物・細胞フラグメント等が混在していることが一般的ですが、QCMを用いれば試料中に存在する解析対象の抗原を迅速に検出・定量できます。
ビオチン-ストレプトアビジン相互作用を利用する手法以外にも、超短UVパルスレーザーの照射によって金素材表面(QCMの水晶振動子薄膜に用いられます)に抗体を一定の配向で固定化できます。抗体のC末端側に存在するトリプトファン残基が照射されたUVエネルギーを吸収し、近傍へのエネルギー移動によってヒンジ領域やFc領域に多く存在するジスルフィド結合が切断されて反応性の高いチオール基が生じることで、金薄膜表面に対するC末端側の結合選択性が高まり、抗体のC末端側が金薄膜表面に優先的に結合します。抗体が抗原と結合しやすい配向に固定化されることで、QCMバイオセンサーの選択性と感度が向上します。
QCMの将来的な用途
QCMは次世代のハイスループットなバイオアッセイを牽引するかもしれない大きな可能性を秘めた技術です。QCMの扱いやすさと優れた選択性や感度があれば、将来的に多様な疾患のベッドサイド診断や解析が可能になると期待されます。QCMは臨床現場にとどまらず、世界各国の研究室で導入が検討されるべき技術といえます。バイオマーカー検証やサンプル解析を効率的にマルチプレックス化するその潜在能力は極めて高く、導入コストを比較的安価に抑えられるという点も非常に魅力的です。
バイオマーカー探索から臨床応用にいたるまで、QCMは研究のありとあらゆる段階で活用できる汎用性を備えています。適切にデザインされたセンサーチップを用意できれば技術的な習熟度に関わらず誰でも測定可能である点は、煩雑な工程や専門知識を伴うウェスタンブロット(WB)やフローサイトメトリー(FC)とは異なるQCM法ならではのアドバンテージです。
WBや免疫蛍光染色(IF)といった半定量的な従来の手法から研究の潮流が移り変わる中で、高度な定量性と感度を備えた新技術が台頭しつつあります。QCMや表面プラズモン共鳴(SPR:Surface Plasmon Resonance)は、アッセイの選択性や感度が大幅に向上した、研究のワークフローを効率化する新技術です。QCMは化学分野で幅広く用いられている一方、生物分野に応用するには多くの検証と検討の余地があり、この技術がどのような可能性を切り開くのか、非常に興味深いと言えます。
参考文献