To dye or not to dye?フローサイトメトリーの細胞生死判定試薬の使い分け
フローサイトメトリー解析に欠かせない細胞生死判定試薬の使い分けをマスターして、信頼性の高い正確な解析データを取得しましょう。
信頼性が高く正確なフローサイトメトリー解析の結果を得るうえで、死細胞の除外は極めて重要なステップです。死細胞は、i)抗体との非特異的結合、ii)生細胞よりも高いレベルの自家蛍光、iii)DNA放出によるクランピング(細胞凝集)等が原因となりデータ解析に干渉します。当然ながら、特に低発現抗原を検出したい場合に死細胞の存在はデータ精度を損なう原因となり、細胞のソーティングにも悪影響を及ぼすことがあります。
データから死細胞を除外するための様々な種類の試薬が販売されており、各試薬にはそれぞれに適切な用途、そしてメリットやデメリットがあります。本稿では、各試薬の原理と解析状況に合わせた適切な選択肢を解説します。
DNA結合色素(死細胞染色試薬)
細胞が死ぬ際は細胞膜や核膜の完全性が喪失し、膜透過性が増大した状態になります。そのような状態になると、ヨウ化プロピジウム(PI:Propidium Iodide)や7-AAD(7-Amino-Actinomycin D)、DAPI(4',6-diamidino-2-phenylindole)等のDNA結合色素は細胞内に浸透しDNAと結合します。DNA結合色素を用いる場合のプロトコールは比較的単純明快で、色素を添加して短時間インキュベーションした後にフローサイトメーターで測定します。サンプル中の細胞は時間の経過に伴い死細胞の割合が増加するため、色素添加から測定までの時間を一定に定める等の工夫を加えてサンプル間の蛍光強度を正確に比較できるよう留意してください。DNA結合色素は生細胞と死細胞の膜透過性の差を利用して細胞の生死を判別しますが、この特徴はデメリットにもなり、固定した後の細胞の生死を区別することはできません。
以下の表は、市販されているDNA結合色素をまとめたものです。
|
ヨウ化プロピジウム |
励起波長:488 / 532 / 561 nm 蛍光波長:617 nm |
二本鎖DNAの塩基対にインターカレーションして結合します。ストークスシフトが大きいため、同じ488 nmレーザーで励起される他の蛍光色素(例:FITC、CoraLite® Plus 488)と併用できます。 |
|
7-AAD |
励起波長:488 / 532 / 561 nm 蛍光波長:647 nm |
二本鎖DNAのG-Cリッチな領域の塩基対にインターカレーションして結合します。ストークスシフトが大きいため、同じ488 nmレーザーで励起される他の蛍光色素(例:FITC、CoraLite® Plus 488)と併用できます。 |
|
DAPI |
励起波長:358 / 405 nm 蛍光波長:461 nm |
最大励起波長は358 nmですが、多くの場合405 nmのバイオレットレーザーで励起します。二本鎖DNAのA-Tリッチな領域に結合します。RNAにも結合し、500 nmで蛍光を検出できますが、蛍光強度は低くなります。 |
細胞を固定する場合の死細胞染色試薬
DNA結合色素は固定処理した細胞を一律に透過してしまうため、固定していない細胞の生死の判断に用いられます。一方で、細胞を固定しても生死を判別できる手法は他に数多く存在します。タンパク質のアミノ基と反応する固定細胞用色素は死細胞・生細胞のどちらも染色しますが、生細胞の場合は細胞膜表層のタンパク質と試薬が結合するのに対し、死細胞の場合は破綻した細胞膜を透過して細胞内のタンパク質とも試薬が反応するため生細胞よりも蛍光強度が強くなり(約50倍)、細胞の生死を正確に判断し細胞の生存率を評価できます(図1)。Zombie Dye™(BioLegend)、Ghost Dye™(Tonbo Biosciences)等の固定可能な細胞生死判定色素は、使用が容易で様々な蛍光波長の色素をラインアップしており、様々なパネル構成に組み込むことができるため広く利用されています。プロテインテックのPhantom Dyeは、7種類の励起/蛍光波長を取り揃えた固定可能な細胞生存率測定色素です。Phantom Dyeは細胞内タンパク質に共有結合するため、ホルムアルデヒドやアルコールを用いて固定した細胞でも、結合を維持し正確な生死判定が可能です。これらの色素は固定していない細胞にも利用可能で、フローサイトメトリーのパネル構成に追加できます。また、R-NH₂ビーズを組み合わせると蛍光補正コントロールとして利用できます。
詳細なプロトコールはPMID 20578108をご覧ください。
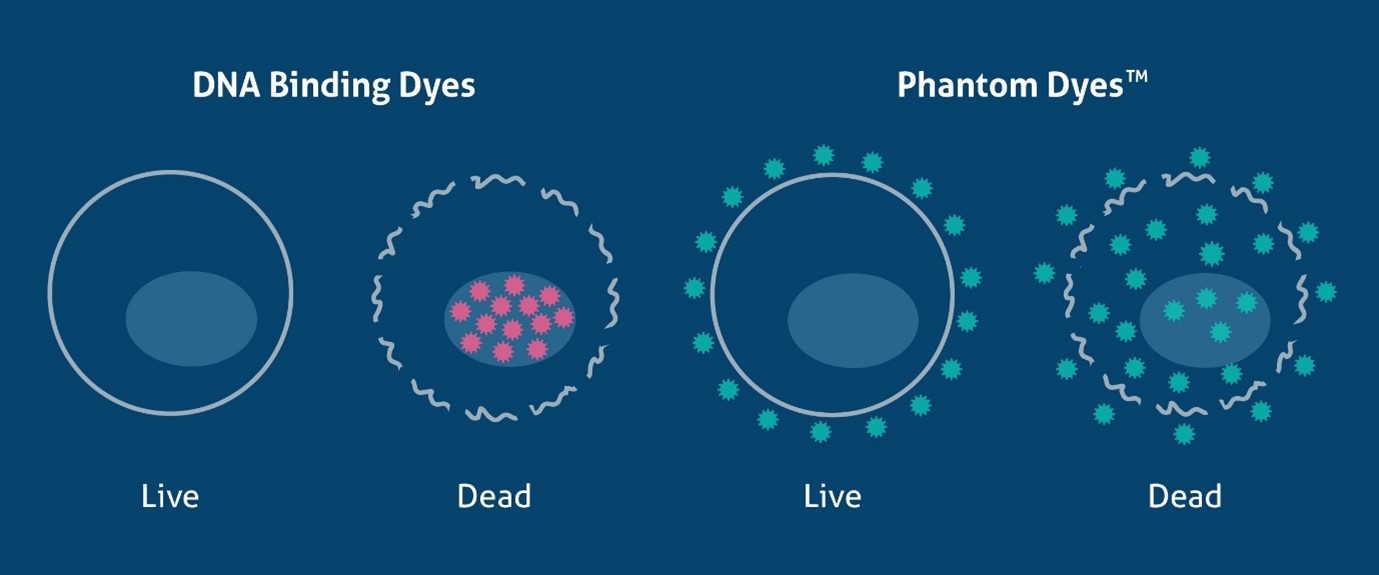
図1. 生細胞と死細胞を区別するメカニズム(DNA結合色素とPhantom Dye(固定細胞用生存率測定色素)の結合様式の概略図)
|
プロテインテックの細胞生存率測定色素「Phantom Dye」
|
Cell health assay
細胞状態の評価キット(Cell health assayキット)を細胞生死判定色素の代わりに利用することもできます。このようなキットで細胞生死判定色素とDNA結合色素を併用して細胞の状態を判定するタイプのキットは、サンプル中の生細胞・死細胞集団の判別にも利用可能で、フローサイトメトリーだけでなく蛍光生細胞イメージングにもよく用いられます。
細胞の生死判定試薬のなかでも代表的な生細胞染色試薬の1つが、非蛍光性の細胞透過性色素であるCalcein AMです。DNA結合色素とは異なり、Calcein AM分子は生細胞を透過すると細胞内エステラーゼの作用によってアセトキシメチルエステルが加水分解され、緑色蛍光を発する蛍光性分子(Calcein anion)に変化します(励起波長:495 nm・蛍光波長:520 nm)。死細胞の場合はエステラーゼ活性がほぼ消失するため、蛍光分子は発生しません。Calcein AMに、Calcein AMとは別の波長で測定するPI(励起波長:488 nm・蛍光波長:617 nm)やEthD-1(励起波長:528 nm・蛍光波長:617 nm)のようなDNA結合色素を組み合わせると、1回のアッセイで死細胞集団を判別するとともに、細胞の生存率や細胞毒性等を評価できます(図2)。酵素等を利用するタイプのアッセイは固定処理した細胞の場合、色素分子が細胞内物質と反応しないため細胞の生死を評価することはできません。キットで処理した未固定サンプルをただちに測定するよう留意してください。
|
プロテインテックの哺乳類細胞生存率測定キット「Viability/Cytotoxicity Assay Kit for Animal Live & Dead Cells」
死細胞の染色にはPIまたはEthD-1のいずれかを選択可能です。 |
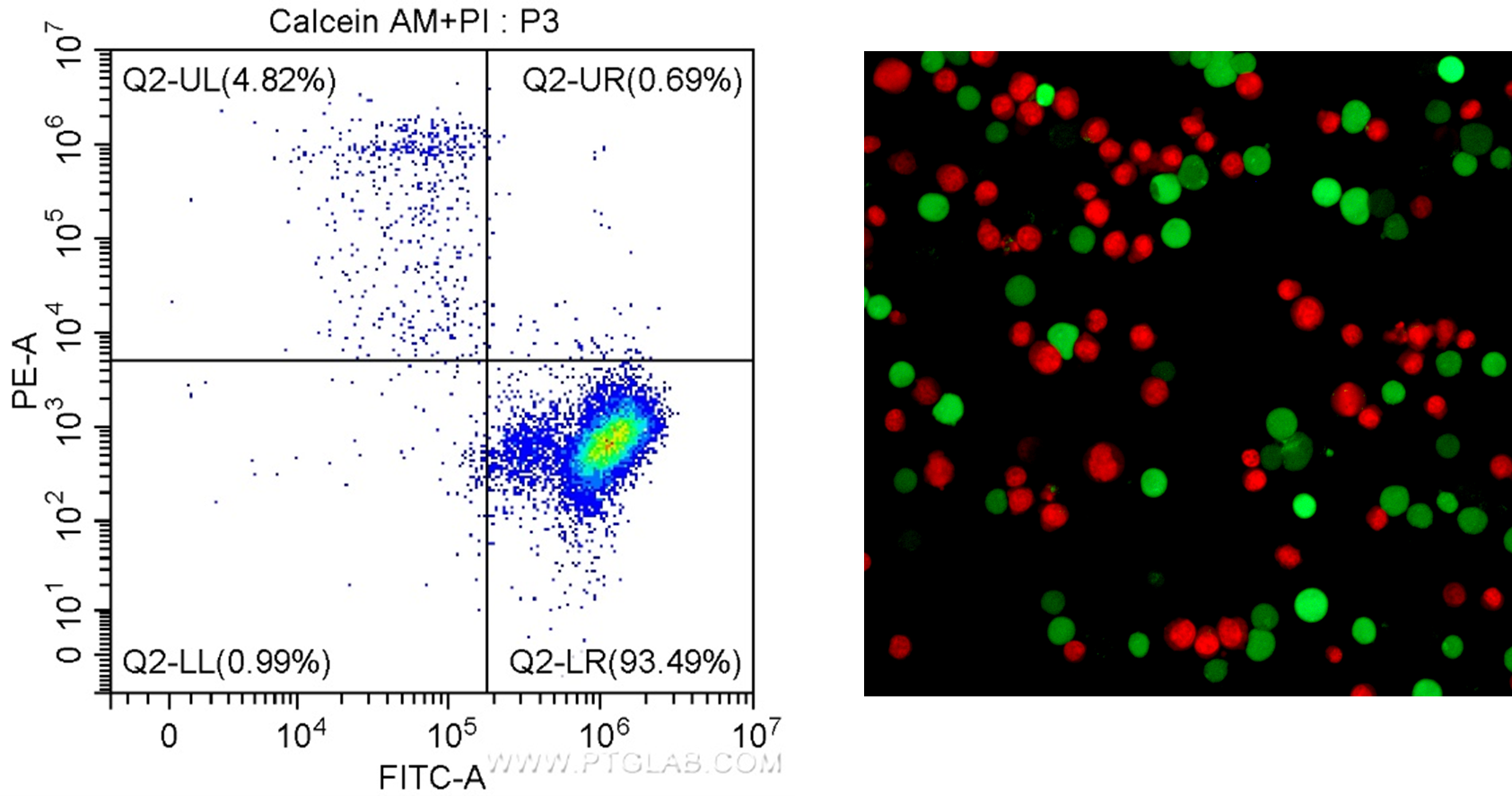
図2. Viability/Cytotoxicity Assay Kit for Animal Live & Dead Cells (Calcein AM, PI Method)(カタログ番号:PF00007)を使用した実験結果。左:フローサイトメトリーで、生細胞はCalcein AM陽性(FITC-A)、死細胞はPI陽性(PE-A)を示します。右:Jurkat細胞をキットで染色し蛍光顕微鏡で撮影すると、Calcein AM染色された生細胞は緑色、PI染色された死細胞は赤色で示されます。
フローサイトメトリーを使用したアポトーシスの検出
アポトーシスは高度に制御された細胞死の一種で、生物の発生や恒常性維持に極めて重要な役割を果たします。アポトーシスの制御不全はがんやアルツハイマー病等の疾患の原因になる可能性があるとされています(アポトーシスに関する詳細な情報についてはブログ「ネクローシス(Necrosis)とアポトーシス(Apoptosis)の違いとは?」をご参照ください)。
フローサイトメトリーはアポトーシス研究に有用なツールでもあり、アポトーシスのプロセスを評価するためのキットや色素のセットが数多く販売されています。なかでも、Annexin VアッセイやTUNELアッセイは広く用いられている手法です。
Annexin Vは、アポトーシス初期段階のマーカーであるホスファチジルセリン(PS:Phosphatidylserine)とCa2+依存的に結合するタンパク質です。生細胞の場合は、細胞質側の細胞膜にPSが存在しますが、アポトーシスの初期段階にPSは細胞膜の外側に反転します。細胞膜の外側に露出したPSは蛍光色素標識Annexin Vと結合するため、フローサイトメトリーや蛍光顕微鏡を用いて蛍光シグナルを測定するとアポトーシス細胞と生細胞を判別できます。
|
プロテインテックのアポトーシス検出用試薬
CoraLite® Plus 488を標識したAnnexin VにPIを併用し、初期段階のアポトーシス細胞や後期段階のアポトーシス細胞を検出できます(図3参照)。 |
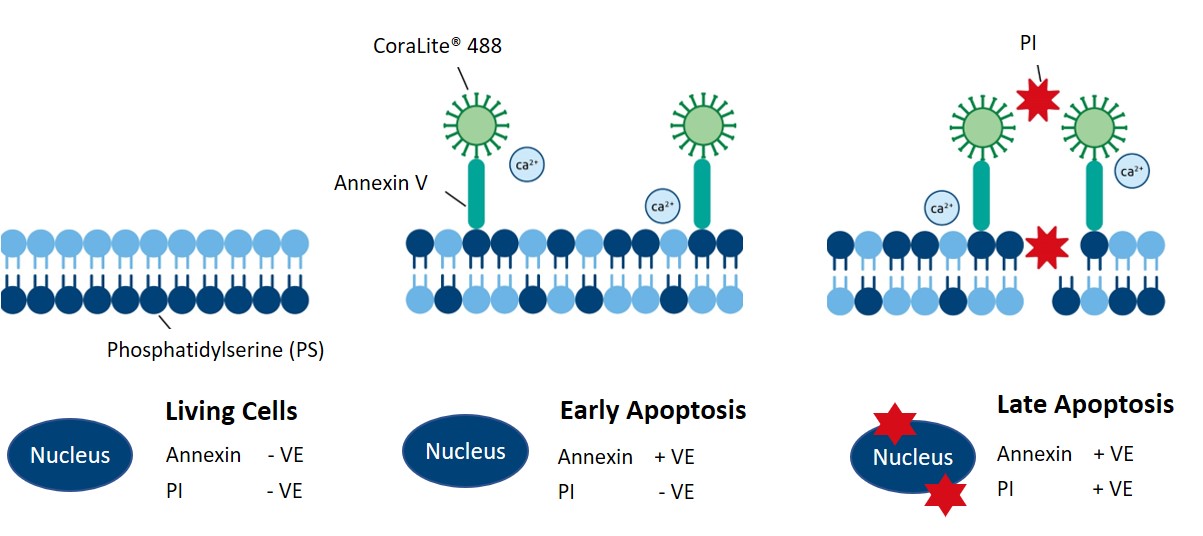
図3. CoraLite® Plus 488-Annexin V and PI Apoptosis Kit(カタログ番号:PF00005)が初期アポトーシス細胞と後期アポトーシス細胞を検出・区別する原理
アポトーシスを評価する別の汎用的な方法に、TUNELアッセイが挙げられます。細胞内の染色体DNAの崩壊はアポトーシスの特徴的な現象で、3'-OH基が露出した180~200 bpの倍数の長さの様々な鎖長のDNA断片が発生し、アポトーシス細胞サンプルから抽出したDNAを電気泳動するとラダー状のパターンが認められます。TUNELアッセイではTdT(Terminal deoxynucleotidyl transferase)という酵素の作用を利用して、蛍光標識dUTPをアポトーシス細胞のDNAフラグメントの3'-OH末端に付加させます。その後、dUTPが付加したDNAの蛍光を蛍光顕微鏡で観察するかフローサイトメトリーで定量します。
|
プロテインテックのアポトーシス検出用試薬「TUNEL Assay Apoptosis Detection Kit」
偶発的な細胞死により生じたネクローシス細胞や、アポトーシス以外の要因でDNA鎖が切断された細胞を適切に除外し、高感度かつ選択的にアポトーシス死細胞を検出します。CoraLite® Plus 488標識dUTP、またはCoraLite® 594標識dUTPのいずれかを選択可能です。 |


