特集 : 肝臓疾患研究
肝臓疾患研究、関連因子について解説します。
目次 |
はじめに
世界全体で、肝臓癌は、最もよく診断される悪性腫瘍の第5位、最も一般的な癌関連死の原因の第3位を占め続けています。肝臓癌の発生率が絶えず増加する一方で、生存率は極めて不良です1,2。肝臓癌は、複数のリスク因子を有するため非常に異質性の高い疾患です(下図を参照)。さらに、肝臓癌の発生メカニズムは非常に複雑であり、複数の段階で生じます。これまで、肝臓癌の原因は十分に解明されておらず、治療のための早期診断マーカーが強く望まれています。そのため、肝臓癌は重大な健康問題であり続けています。本稿では、肝疾患の研究を促進・支援するために、いくつかのよく使用されるマーカーについて概説するとともに、肝臓癌の新規標的にも焦点を当てています。
肝臓癌の原因
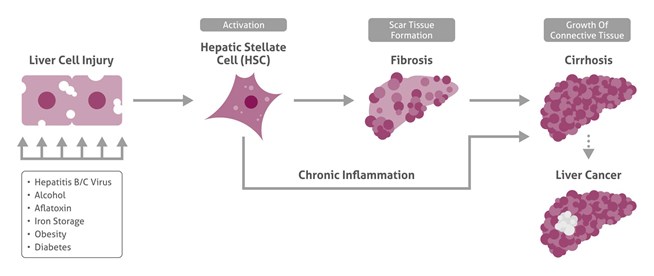
複雑な肝臓の多数の標的
肝臓は体内で最大の腺性器官です。この複雑な臓器は、生存に極めて重要な複数の機能を果たします(表1を参照)。全ての肝臓疾患(そのうち最も重要なのは肝臓癌です)について、その発生を多段階のプロセスとして理解する必要があります。様々なシグナル伝達経路の変化、あるいは制御遺伝子の遺伝的およびエピジェネティックな変化の結果として癌遺伝子の活性化または不活性化が無制御になることが肝臓癌の発生に関与していますが、正確な相互作用は今日でも十分に解明されていません3, 4。
Wntシグナル伝達のメカニズムについては、多数の出版物で論じられてきました。Wnt経路とその成分(例えばβ-カテニン(カタログ番号:51067-2-AP))の変化は、肝臓癌形成において極めて重要であることが立証されています5, 6。多機能タンパク質であるβ-カテニンは、シグナル伝達媒介物質で、通常の条件では細胞質に存在し、継続的に分解します。IHCによる核β-カテニンの検出は、β-カテニン転写活性を示すと一般的に考えられています。ヒト肝臓疾患および肝臓関連疾患の分子解析は、複数の研究において、異なるSmadを介したトランスフォーミング増殖因子β(TFF-β(カタログ番号:18978-1-AP))依存性シグナル伝達7の重要性も示しています。TGF-βは、肝臓疾患の中心的な調節因子と考えられており、疾患の進行の全ての段階に寄与します。例えば、Smad7(カタログ番号:25840-1-AP)は負のフィードバックループを介してTGF-βシグナル伝達を阻害することが知られており、Smad3(カタログ番号:25494-1-AP)は転写応答の調節に重要な役割を果たします。肝細胞増殖因子シグナル伝達経路も、正常肝臓、肝再生、または腫瘍形成過程において同様に重要です。
| SMAD7 | |
 |
 |
|
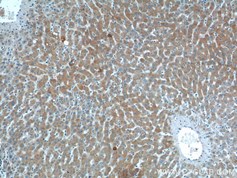
Smad7(カタログ番号:25840-1-AP、希釈倍率:1:200)抗体を使用したパラフィン包埋ヒト肝組織のIHC染色(10倍対物レンズ)。 |
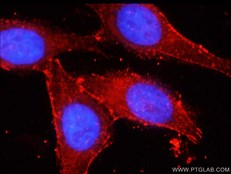
βカテニン(カタログ番号:51067-2-AP、希釈倍率:1:50)抗体を使用したHepG2細胞の免疫蛍光分析。 |
表1
| 肝機能の概要 |
| 有害物質の除去 |
| 食物の貯蔵・消化 |
| 食物を体に必要な低分子量物質に変換 |
| シグナル伝達分子と血漿タンパク質の合成 |
肝臓疾患インフォグラフィック: ダウンロードはこちら |
関連製品
| 抗体名 | カタログ番号 | アプリケーション |
| Beta-Catenin | 51067-2-AP | ELISA, WB, IP, IHC, IF, FC, CoIP, ChIP |
| Hepatocytes Growth Factor (HGF) | 10390-1-AP | ELISA, WB, IP, IHC, IF |
| TGF-ß | 18978-1-AP | ELISA, WB, IHC, Cell treatment |
| TGF-ß | 21898-1-AP | ELISA, WB, IP, IHC, IF, FC, CoIP, Cell treatment |
| Smad3 | 25494-1-AP | ELISA, WB, IHC, IF |
| Smad7 | 25840-1-AP | ELISA, WB, IP, IHC, IF, CoIP |
肝星細胞の活性化
肝星細胞(HSC:hepatic stellate cells)の活性化は、主要な線維形成メカニズムの1つと考えられています。正常な肝臓では、HSCは休止状態にあり、ビタミンAの主な貯蔵場所になっていますが、肝線維化の過程で主要なマトリックス産生細胞になります。
α平滑筋アクチン(α-SMA)(カタログ番号:14395-1-AP)とデスミン(カタログ番号:60226-1-Ig、16520-1-AP)の出現は、HSCの活性化を示し、これらはHSCのステージを特定する免疫染色によく使用されます8, 9。シナプトフィシンは二重染色に適しており、前述の二者と異なり、休止状態と活性化状態の両方のHSCの表面に発現しています10。
HSC活性化の調節には複数のサイトカインが関与しており、HSCの活性化によって線維化が誘発されるので、多くの抗線維化療法は、HSCの活性化を促進するメカニズムの解明に着目しています。
関連製品
| 抗体名 | カタログ番号 | アプリケーション |
| Rabbit Anti Smooth Muscle Actin | 55135-1-AP | ELISA, WB, IHC, IF |
| ACTA2 | 23081-1-AP | ELISA, WB, IP, IHC, IF |
| Desmin | 60226-1-lg | ELISA, WB, IHC, IF |
| Desmin | 16520-1-AP | ELISA, WB, IP, IHC, IF, FC |
| Synaptophysin | 17785-1-AP | ELISA, WB, IP, IHC, IF |
線維症
肝線維症は、慢性肝障害の結果、すなわち肝臓の反復損傷に対する創傷治癒反応です。肝損傷が持続すると、肝再生が正常に起こらず、アポトーシスを起こした肝細胞が大量のECMタンパク質に置き換わります。したがって、細胞外マトリックス(ECM)タンパク質の過剰蓄積は、肝線維症の特徴です。
例えば、この段階で肝臓のECMタンパク質様コラーゲン(コラーゲンIII、カタログ番号:13548-1-AP)含量は約6倍多くなります。肝線維症が進行すると、これらのコラーゲンバンドは架橋し始め、肝硬変の段階に達します(次章を参照)。活性化された肝星細胞、門脈線維芽細胞、または筋線維芽細胞は、線維化した肝臓における主要なコラーゲン産生細胞であることが知られています(肝細胞の概要を表2に示します)。
結合組織増殖因子(CTGF:Connective Tissue Growth Factor、23936-1-AP)は、組織改造において中心的役割を果たし、肝線維化過程で上皮間葉転換(EMT)を促進する主要標的であると報告されています。CTGFは、増殖、分化、およびECM合成にも関与します11, 12, 13。CTGFは単独で作用することもできますが、様々なサイトカインの発現を誘導することもできます。例えば、CTGFは血管内皮増殖因子(VEGF、カタログ番号:19003-1- AP)14の発現を誘導し、VEGFにより、CTGFの発現がより多く誘導されます。VEGFには、線維化促進分子の放出を増加させる他、多様な線維形成効果があり、血管新生機能と炎症促進作用も持ちます。
肝線維症は、慢性肝疾患が肝硬変へと進行する際の一般的な経路です。肝線維症とその標的を継続的に解明することは、線維化メカニズムの完全な理解をもたらすのに役立ちます。
 |
 |
|
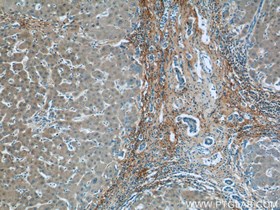
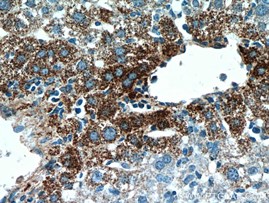
コラーゲンIII(カタログ番号:13548-1-AP、希釈倍率:1:100)抗体を使用したパラフィン包埋ヒト肝硬変組織のIHC染色(10倍対物レンズ)。 |
コラーゲンIII(カタログ番号:13548-1-AP、希釈倍率:1:50)抗体を使用した、パラフィン包埋マウス肝臓のIHC染色(40倍対物レンズ) |
 |
 |
|
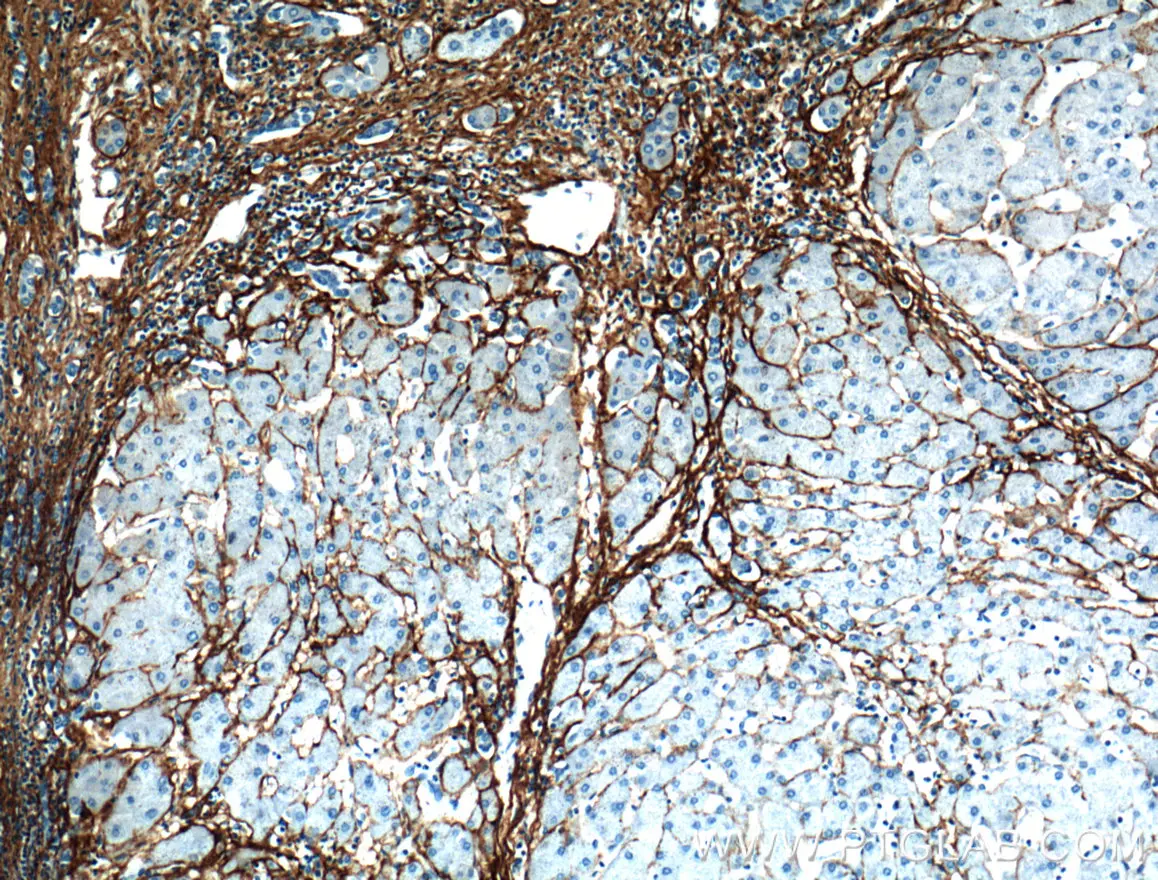
コラーゲンIII(カタログ番号:22734-1-AP、希釈倍率:1:1000)抗体を使用したパラフィン包埋ヒト肝硬変組織のIHC染色(10倍対物レンズ)。 |
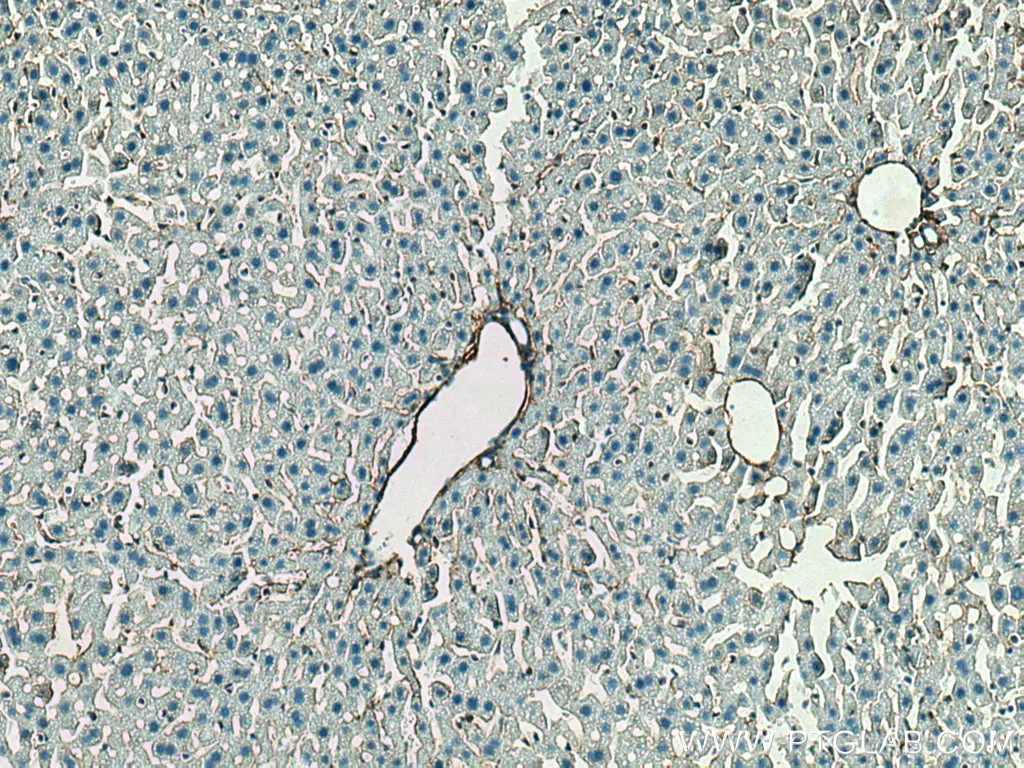
コラーゲンIII(カタログ番号:22734-1-AP、希釈倍率:1:1000)抗体を使用した、パラフィン包埋マウス肝臓スライドのIHC染色(10倍対物レンズ)。Tris-EDTAバッファー(pH9)で加熱抗原賦活化を行った。 |
表2
| 肝臓を構成する様々な細胞種 |
| 肝細胞 |
| 肝星細胞 |
| 前駆細胞 |
| 胆管細胞 |
| クッパー細胞 |
| 内皮細胞 |
肝硬変
肝線維症が進行すると肝硬変に至ります。肝硬変は、構造崩壊、肝細胞再生の変化、および血管変化を特徴とします。肝硬変は、肝不全と門脈圧亢進症のリスク増加とも関連しており、多くの場合肝移植が必要です15, 16。肝硬変は生命に関わる合併症につながることがあるので、その正確な評価が重要です。慢性肝疾患を促進する炎症性シグナル伝達の大きな寄与についてはまだ完全には理解されていませんが、1つだけ挙げるとすると、リンホトキシンβ受容体(LTβR)(カタログ番号:20331-1-AP)を介したシグナル伝達があります。線維症または肝硬変が存在する場合に、複数の種類の肝臓細胞で慢性肝障害時にLTβRが過剰発現することが報告されており17、LT-β受容体の活性化により、炎症を促進するケモカインと接着分子の産生が誘導されます18。
加えて、肝血管新生と類洞の毛細血管化は、肝硬変が進行する過程における主要な特徴です。CD34(カタログ番号:14486-1-AP)陽性内皮細胞の発現は、肝硬変における血管新生プロセスを理解する上で重要な役割を果たします19。類洞の毛細血管化は、内皮細胞間のタイトジャンクションの形成と新血管の形成を伴って進行します。CD31(カタログ番号:11265-1-AP)は、毛細血管単位を検出する特異的かつ高感度のマーカーです19。肝硬変のプロセスを理解することは、癌に進行する前にこの肝障害を治療する効率的な方法の設計に役立つ可能性があります。www.ptglab.co.jpにアクセスして、関心のあるマーカーを選択してください。
関連製品
| 抗体名 | カタログ番号 | アプリケーション |
| LTBR | 20331-1-AP | ELISA, WB, IHC, IF, FC |
| CD34 | 60180-1-Ig | ELISA, WB, IHC, IF, FC |
| CD31 | 11265-1-AP | ELISA, WB, IP, IHC, IF, FC, Cell treatment |
肝臓癌
肝細胞癌(HCC)は主要な死因の一つであり、世界で5番目に多い癌です。進行が急速で治療法が限られているので、早期の診断と介入が不可欠です。
一般的に使用されるバイオマーカーの例として、α–フェトプロテイン(AFP)(カタログ番号:14550-1-AP)、アルブミン(カタログ番号:16475-1-AP)、アルギナーゼ-1(カタログ番号:16001-1-AP、66129-1-Ig)、ビメンチン(カタログ番号:10366-1-AP)、(カタログ番号:17513-1-AP)、炭酸脱水酵素9(カタログ番号:11071-1-AP、66243-1-Ig)、グルタミンシンテターゼ(カタログ番号:11037-2-AP)、E-カドヘリン(カタログ番号:20648-1-AP)が挙げられます。しかしながら、この疾患は複雑であるため、疾患の原因の理解を深めるために新しい因子が絶えず報告されています。
通常多くのヒト組織の上皮細胞で発現しているゴルジタンパク質-73(GP73)を用いた新しいマーカーが報告されています。GP73はヒトの生存に不可欠であり、肝臓で複数の細胞機能を果たしています。GP73の発現は、肝疾患患者の血清サンプルで亢進しており、HCCで発現が最も著しくなっています20。
甲状腺転写因子(TTF)-1(カタログ番号:66034-1-Ig)も過去数年の間に発見された非常に有用な腫瘍マーカーであり、原発癌と転移性肝癌との鑑別に役立つ可能性があります21。S100A6(カタログ番号:10245-1-AP)とFUCA1(カタログ番号:16420-1-AP)は、ヒト肝細胞癌において細胞増殖と遊走を促進するので、これらの高値は転帰不良と関連付けられています22, 23。例えば、グリピカン3(GPC3)(カタログ番号:25175-1-AP)は、肝細胞癌(HCC)の新規マーカーとして最近報告されており、GPC3に依存する腫瘍増殖阻害と、GPC3の免疫療法における治療標的としての可能性が示唆されています24。
近年、早期診断と分子肝発癌に関する知見の増加に関して大きな進歩が遂げられました。これらの成果は、新たな標的療法機会の提供に役立ちます。
 |
 |
|
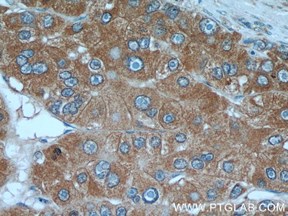
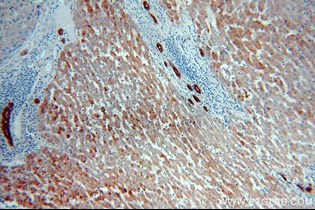
α-フェトプロテイン(AFP)(カタログ番号:14550-1-AP、希釈倍率:1:50)を使用したパラフィン包埋ヒト肝癌のIHC染色(40倍対物レンズ)。 |
サイトケラチン特異的(CK7)(カタログ番号:17513-1-AP、希釈倍率:1:50)抗体を使用したパラフィン包埋ヒト肝臓のIHC染色(10倍対物レンズ) |
 |
 |
|
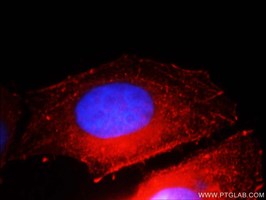
E-カドヘリン(カタログ番号:20648-1-AP、希釈倍率:1:25)抗体、ローダミン標識ヤギ抗ウサギIgG(赤)およびDAPI(青)を使用したHepG2細胞の免疫蛍光染色。 |
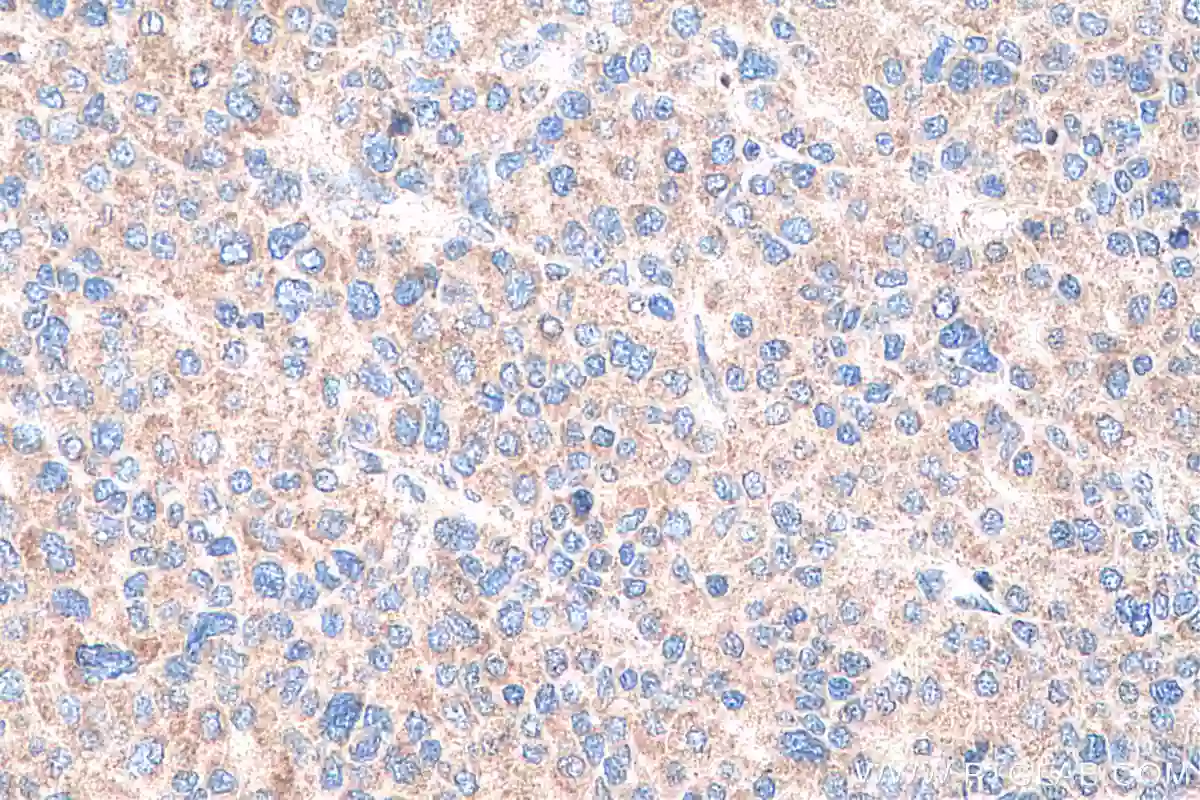
グリピカン3(GPC3)(カタログ番号:25175-1-AP、希釈倍率:1:500)抗体を使用したパラフィン包埋ヒト肝癌組織スライドのIHC染色(40倍対物レンズ)。Tris-EDTAバッファー(pH9)で加熱抗原賦活化を行った。 |
関連製品
| 抗体名 | カタログ番号 | アプリケーション |
| α-Fetoprotein (AFP) | 14550-1-AP | ELISA, WB, IP, IHC, IF, FC, CoIP |
| Albumin | 16475-1-AP | ELISA, WB, IP, IHC, IF, CoIP |
| Arginase-1 | 16001-1-AP | ELISA, WB, IP, IHC, IF, FC |
| Arginase-1 | 66129-1-lg | ELISA, WB, IP, IHC, IF |
| CA9 | 11071-1-AP | ELISA, WB, IP, IHC, IF, FC |
| CA9 | 66243-1-lg | ELISA, WB, IHC, IF, FC |
| Cytokeratin 7 | 17513-1-AP | ELISA, WB, IP, IHC, IF, FC |
| E-Cadherin | 20648-1-lg | ELISA, WB, IHC, IF, FC |
| FUCA1 | 16420-1-AP | ELISA, WB, IHC |
| Glutamine Synthetase | 11037-2-AP | ELISA, WB, IP, IHC, IF, FC |
| Glypican 3 (GPC3) | 25175-1-AP | ELISA, WB, IP, IF |
| GP73 | 15126-1-AP | ELISA, WB, IP, IHC, IF, FC |
| HSP70 | 10995-1-AP | ELISA, WB, IP, IHC, IF, FC, CoIP, Cell treatment |
| S100A6 | 10245-1-AP | ELISA, WB, IP, IHC, IF, FC |
| TTF-1 | 66034-1-lg | ELISA, WB, IHC, IF |
| Vimentin | 10366-1-AP | ELISA, WB, IP, IHC, IF, FC, CoIP |
肝臓疾患研究の製品カタログはこちら(PDF) |
参考文献
- Bruix, J., et al., Focus on hepatocellular carcinoma. Cancer Cell, 2004. 5 (3): pp. 215–9.
- El–Serag, H.B. and A.C. Mason, Rising incidence of hepatocellular carcinoma in the United States. N Engl J Med, 1999. 340 (10): pp. 745–50.
- Tischoff, I. and A. Tannapfe, DNA methylation in hepatocellular carcinoma.World J Gastroenterol, 2008. 14 (11): pp. 1741–8.
- Burroughs, A., D. Hochhauser, and T. Meyer, Systemic treatment and liver transplantation for hepatocellular carcinoma: two ends of the therapeutic spectrum. Lancet Oncol, 2004. 5 (7): pp. 409–18.
- Llovet, J.M., A. Burroughs, and J. Bruix, Hepatocellular carcinoma. Lancet, 2003. 362 (9399): pp. 1907–17.
- Veeman MT, Axelrod JD, Moon RT., A second canon. Functions and mechanisms of beta-cateninindependent Wnt signaling. Dev Cell. 2003; 5 (3): pp. 367–377
- Farazi, Pp. A. and R.A. DePinho, Hepatocellular carcinoma pathogenesis: from genes to environment. Nat Rev Cancer, 2006. 6 (9): pp. 674–87.
- Yu E, Choe G, Gong G, Lee I., Expression of alpha–smooth muscle actin in liver diseases, J Korean Med Sci. 1993 Oct; 8 (5): pp. 367–73.
- Mabuchi A, Mullaney I, Sheard PW, Hessian PA, Mallard BL, Tawadrous MN, Zimmermann A, Senoo H, Wheatley AM, Role of hepatic stellate cell/hepatocyte interaction and activation of hepatic stellate cells in the early phase of liver regeneration in the rat. J Hepatol. 2004 Jun;40(6):910–6.
- Cassiman D., Libbrecht L., Desmet V., Denef C., Roskams T., Hepatic stellate cell/ myofibroblast subpopulations in fibrotic human and rat livers, 2002) Journal of Hepatology. 36(2). pp. 200–209.
- Abreu J G, Ketpura N I, Reversade B, De Robertis E, M. Connective–tissue growth factor (CTGF) modulates cell signaling by BMP and TGF–beta. Nat Cell Biol 2002, 4: pp. 599–604.
- Grotendorst GR, Rahmanie H, Duncan MR: Combinatorial signaling pathways determine fibroblast proliferation and myofibroblast differentiation. FASEB J 2004, 18: pp. 469–479.
- Lee CH, Shah B, Moioli EK, Mao JJ: CTGF directs fibroblast differentiation from human mesenchymal stem/stromal cells and defines connective tissue healing in a rodent injury model. J Clin Invest 2010, 120: pp. 3340–3349.
- Gerber HP, Dixit V, Ferrara N. Vascular endothelial growth factor induces expression of the antiapoptotic proteins Bcl–2 and A1 in vascular endothelial cells. J Biol Chem 1998; 273: 13313.
- Hernandez–GeaV,FriedmanSL. Pathogenesisofliverfibrosis. Annu Rev Pathol, 2010; 6: pp. 425–456.
- Fattovich G, Giustina G, Degos F, Tremolada F, Diodati G, Almasio Pet al. Morbidity and mortality in compensated cirrhosis type C: a retrospective follow–up of 384 patients. Gastroenterology 1997; 112: pp. 463–472.
- Degli–Esposti MA, Davis–Smith T, Din WS, et al. Activation of the lymphotoxin ß receptor by crosslinking induces chemokine production and growth arrest in A375 melanoma cells. J Immunol 1997; 158: pp. 1756–62
- Ngo VN, Korner H, Gunn MD, et al. Lymphotoxin alpha/beta and tumour necrosis factor are required for stromal cell expression of homing chemokines in B and T cell areas of the spleen. J Exp Med 1999; 189: pp. 403–12.
- 9 Pusztaszeri M, Chaubert P, Bosman FT, Seelentag W. Immunohistochemical expression expression of endothelial markers CD31, CD34, von–Willebrand factor and Fli–1 in normal human tissues. J Histochem Cytochem 2006; 54: pp. 385–95.
- Ba M–C., Long H., Tang Y–Q., Cui Z–H. GP73 expression and its significance in the diagnosis of hepatocellular carcinoma: a review, Int J Clin Exp Pathol. 2012; 5(9): pp. 874–881.
- Wieczorek TJ, Pinkus JL, Glickman JN. Comparison of thyroid transcription factor–1 and hepatocyte antigen immunohistochemical analysis in the differential diagnosis of hepatocellular carcinoma, metastatic adenocarcinoma, renal cell carcinoma, and adrenal cortical carcinoma. Am J Clin Pathol. 2002; 118: pp. 911–921.
- Miyoshi E., Noda K., Taniguchi N., Sasaki Y., Hayashi N., Significance of α1–6 Fucosylation in Hepatocellular Carcinoma, Springer, 2001, pp. 93–104.
- Feng M, Ho M.,, Glypican–3 antibodies: a new therapeutic target for liver cancer, FEBS Lett. 2014 Jan 21; 588 (2): pp. 377–82.
- 4 Ho M, Kim H., Glypican–3: a new target for cancer immunotherapy, Eur J Cancer. 2011 Feb; 47 (3): pp. 333–8.
| GAPDH 抗体 | 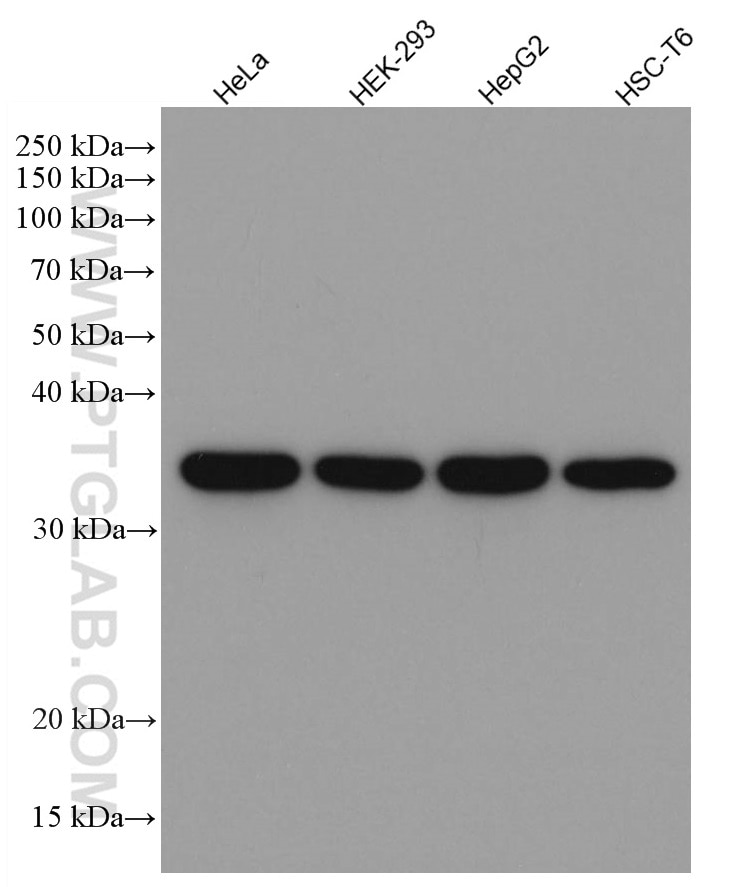 |
| カタログ番号:60004-1-Ig | |
|
GAPDH酵素は、広い細胞種で高く発現するため、ウエスタンブロット実験におけるタンパク質ローディングコントロールとして頻繁に使用されます。GAPDHは、解糖、DNA修復、アポトーシス等、いくつかの細胞機能にも関わることが知られています。 プロテインテックのモノクローナルGAPDH抗体は、ヒト全長タンパク質に対して作製されており、これまでに9,042報以上の文献で使用されています。 |
| Beta Actin 抗体(KD/KO 検証済) |  |
| カタログ番号:66009-1-Ig | |
|
ベータアクチンは、全ての真核細胞タイプにわたって広範で一貫した発現を示し、また、このタンパク質の発現レベルはほとんどの実験的処理に影響を受けないことから、通常、ローディングコントロールとして用いられます。 66009-1-Igは、これまでに4,969 報以上で使用されており、様々な動物種で使用できます。 |
